據(jù)美國(guó)糖尿病協(xié)會(huì)估計(jì),全世界每 30 秒就有一條腿被截肢,其中 85% 是由糖尿病足潰瘍并發(fā)癥引起。我國(guó) 50 歲以上的糖尿病患者,糖尿病足的發(fā)病率高達(dá) 8.1%,而糖尿病足潰瘍(DFU)患者年死亡率高達(dá) 11%。
根據(jù)國(guó)際健康與臨床標(biāo)準(zhǔn)化治療策略,早期有效的糖尿病足管理可以大幅降低并發(fā)癥的嚴(yán)重程度,顯著減低截肢率和死亡率,提高患者生活質(zhì)量。根據(jù)目前大量研究顯示,促進(jìn)糖尿病足愈合的治療方法主要有:血糖控制、傷口清創(chuàng)、敷料護(hù)理治療、血運(yùn)重建手術(shù)、高壓氧治療、電刺激、負(fù)壓傷口治療、生物工程皮膚和生長(zhǎng)因子應(yīng)用。
01 什么是糖尿病足?
糖尿病足是指糖尿病患者由于并發(fā)下肢神經(jīng)病變及不同程度周圍血管病變而導(dǎo)致的足部感染、足部潰瘍和/或深部組織破壞。其中糖尿病足的潰瘍連續(xù)性、可重復(fù)性和不愈合性是這種并發(fā)癥的主要特征,也是糖尿病患者下肢截肢的主要原因。
目前糖尿病足尚無(wú)有效治療方法,患者會(huì)發(fā)生反復(fù)感染和無(wú)法愈合的潰瘍,最終不得不接受截肢,其已成為嚴(yán)重危害人類健康的疾病之一,迫切需要研發(fā)有效治療手段。干細(xì)胞療法的誕生為處于困境之中的糖尿病足點(diǎn)燃了治療的新希望,越來越多的研究正在證實(shí)干細(xì)胞療法治療糖尿病足的安全性與有效性。
02 干細(xì)胞有望成為治療糖尿病足新方法
近日,國(guó)際研究者在 world journal of plastic surgery 雜志上發(fā)表了關(guān)于間充質(zhì)干細(xì)胞治療糖尿病足的綜述,分析了 22 篇與間充質(zhì)干細(xì)胞治療糖尿病足潰瘍相關(guān)的研究論文,表明間充質(zhì)干細(xì)胞通過旁分泌信號(hào)和誘導(dǎo)分化機(jī)制在糖尿病足的皮膚再生和傷口愈合中發(fā)揮有益作用。

通常,傷口愈合過程是幾個(gè)步驟相互作用過程,最終導(dǎo)致功能性真皮、表皮層的修復(fù)和血運(yùn)重建。傷口創(chuàng)傷愈合的基本過程:急性炎癥期→細(xì)胞增生期→瘢痕形成期→表皮及其它組織再生。
急性炎癥期:表現(xiàn)為充血、漿液滲出、中性粒細(xì)胞和巨噬細(xì)胞游出。傷口中的血液和滲出液中的纖維蛋白原凝固形成凝塊、痂皮,凝塊及痂皮保護(hù)傷口。
細(xì)胞增生期:急性炎癥期后傷口邊緣的整層皮膚及皮下組織由于傷口邊緣新生的肌成纖維細(xì)胞的牽拉作用向中心移動(dòng),使傷口迅速縮小。5-羥色胺(5-HT)、血管緊張素及去甲腎上腺素能促進(jìn)傷口收縮。
瘢痕形成期:從傷口底部及邊緣長(zhǎng)出肉芽組織(提供上皮再生所需的營(yíng)養(yǎng)及生長(zhǎng)因子),填平傷口;新生毛細(xì)血管增長(zhǎng);成纖維細(xì)胞產(chǎn)生膠原纖維,隨著膠原纖維越來越多,出現(xiàn)瘢痕,最終瘢痕與皮膚表面平行。
表皮及其他組織再生:傷口邊緣的表皮基底增生,并在凝塊下面向傷口中心移動(dòng),形成單層上皮,覆蓋于肉芽組織的表面,并增生、分化成為鱗狀上皮。
03 間充質(zhì)干細(xì)胞促進(jìn)糖尿病足的血管生成
再生醫(yī)學(xué),特別是那些使用干細(xì)胞的療法,越來越多地被引入用于傷口愈合的治療方法中。間充質(zhì)干細(xì)胞具有強(qiáng)大的增殖能力、分化能力以及低水平的免疫排斥反應(yīng),在合適的環(huán)境下,其可以分化成各種細(xì)胞類型。
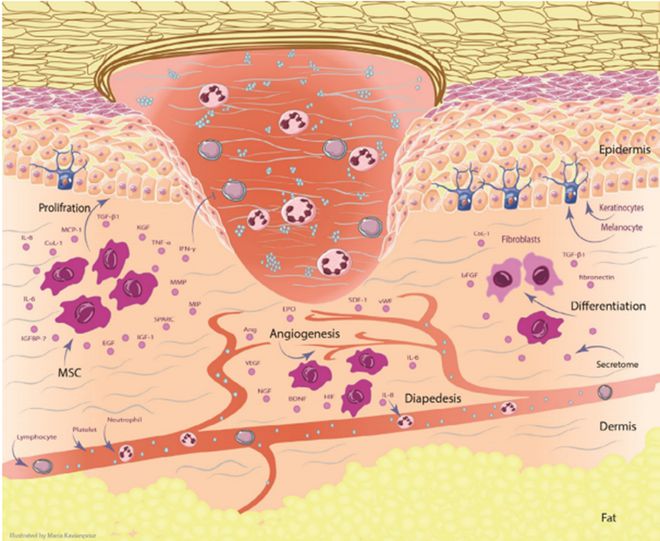
注:間充質(zhì)干細(xì)胞及其分泌作用在糖尿病足皮膚破潰治療中的作用
如圖所示,間充質(zhì)干細(xì)胞通過以下過程促進(jìn)糖尿病足創(chuàng)面的愈合。
間充質(zhì)干細(xì)胞可通過分泌血管內(nèi)皮生長(zhǎng)因子(VEGF)、神經(jīng)生長(zhǎng)因子(NGF)、腦源性神經(jīng)營(yíng)養(yǎng)因子(BDNF)、血管生成素(Ang)、基質(zhì)細(xì)胞衍生因子-1(SDF-1)、血管性血友病因子(vWF)、促紅細(xì)胞生成素(EPO)和缺氧誘導(dǎo)因子(HIF)遷移至傷口破潰處并促進(jìn)血管新生。
間充質(zhì)干細(xì)胞通過調(diào)節(jié)胰島素樣生長(zhǎng)因子-1(IGF-1)、表皮生長(zhǎng)因子(EGF)、基質(zhì)金屬蛋白酶(MMP)、轉(zhuǎn)化生長(zhǎng)因子(TGF-β)、角質(zhì)細(xì)胞生長(zhǎng)因子(KGF)、單核細(xì)胞趨化蛋白-1(MCP-1)和金屬蛋白酶的組織抑制劑(TIMP)來改善角質(zhì)形成細(xì)胞的功能。
間充質(zhì)干細(xì)胞可通過膠原蛋白-1(Col-1)、轉(zhuǎn)化生長(zhǎng)因子(TGF-β)、纖維連接蛋白和堿性成纖維細(xì)胞生長(zhǎng)因子(bFGF)的產(chǎn)生向成纖維細(xì)胞分化。
04 間充質(zhì)干細(xì)胞治療后傷口完全閉合率達(dá)到了82%
近年來,國(guó)內(nèi)外均有針對(duì)糖尿病足潰瘍的間充質(zhì)干細(xì)胞在研產(chǎn)品取得進(jìn)展。2019 年,韓國(guó) Anterogen 研發(fā)了一款含脂肪間充質(zhì)干細(xì)胞的藥物 Allo-ASC-DFU 用于治療糖尿病足潰瘍,其 II 期臨床研究成果已發(fā)表。

該 II 期臨床試驗(yàn)共入駐了 59 位糖尿病足潰瘍患者,分為治療組(采用間充質(zhì)干細(xì)胞片治療)以及對(duì)照組(采用聚氨酯薄膜治療)。每周將同種異體脂肪間充質(zhì)干細(xì)胞片或聚氨酯膜用于糖尿病患者傷口之上。在 1-12 周的每周隨訪中對(duì)傷口進(jìn)行評(píng)估。通過評(píng)估患者的完全閉合的 Kaplan-Meier 中位時(shí)間、傷口完全閉合率、糖尿病足 Wagner 分級(jí)來判斷患者傷口情況。
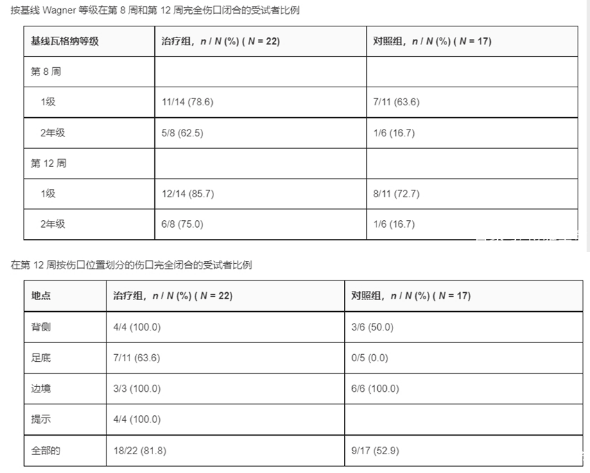
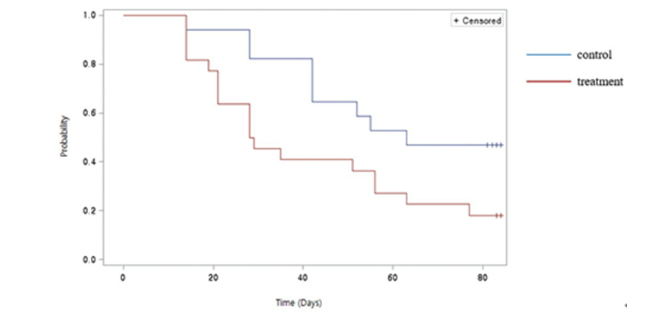
研究發(fā)現(xiàn)治療組的完全閉合的 Kaplan-Meier 中位時(shí)間僅為 28.5 天,而對(duì)照組則需要 63 天。在第 12 周的時(shí)候,治療組傷口完全閉合率達(dá)到了 82%,而對(duì)照組的傷口晚期閉合率只有 53%。此外,Wagner 分級(jí)表示治療組患者的恢復(fù)更快。
在治療期間,患者沒有出現(xiàn)嚴(yán)重的不良事件,在完成治療后繼續(xù)觀察了兩年,隨訪發(fā)現(xiàn)兩組患者均未出現(xiàn)與傷口治療相關(guān)的不良事件,肯定了間充質(zhì)干細(xì)胞治療的安全性以及有效性。
05 干細(xì)胞治療糖尿病足臨床研究
在國(guó)內(nèi),2004 年我國(guó)谷涌泉等最先報(bào)道了采用移植自體骨髓干細(xì)胞治療糖尿病足,并且獲得較好效果。之后,解放軍第三軍醫(yī)大學(xué)西南醫(yī)院的臨床研究納入住院確診的糖尿病足患者 40 例,經(jīng)體外擴(kuò)增自體骨髓間充質(zhì)干細(xì)胞移植后,患者肢體疼痛、冷感、間歇性跛行均有所改善,踝肱指數(shù)明顯升高,雙下肢血管顯像血流灌注有所增加,所有患者創(chuàng)面在治療后 2-4 周內(nèi)均完全愈合。
我國(guó)已有開展干細(xì)胞療法針對(duì)糖尿病足的臨床研究,截至2022年11月,干細(xì)胞臨床研究備案項(xiàng)目中,有3個(gè)與糖尿病足相關(guān)。由此可見,我國(guó)干細(xì)胞治療糖尿病足的臨床研究正在有序發(fā)展當(dāng)中。
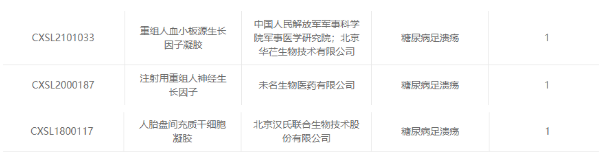
目前,利用干細(xì)胞來治療糖尿病及其并發(fā)癥的臨床研究正在廣泛開展,相信未來,更多的糖尿病患者會(huì)受益于此項(xiàng)技術(shù)。
免責(zé)聲明:
我們尊重原創(chuàng),也注重分享。圖文來源網(wǎng)絡(luò),版權(quán)歸原作者所有,如涉及作品內(nèi)容、版權(quán)或其它問題,請(qǐng)聯(lián)系我們刪除!


 閩公網(wǎng)安備 35020602002648 號(hào)
閩公網(wǎng)安備 35020602002648 號(hào) QQ 客服
QQ 客服
