不久前,瑞士 Agora 轉化癌癥研究中心的 Douglas Hanahan 教授根據 2011 年版介紹了四種新的癌癥特征,以解釋惡性腫瘤發生、發展和治療響應特性的機制。

2022 年 1 月出版的國際頂級刊物 Cancer Discovery(IF=39)封面上是一個“金色指環”,指環側面鑲嵌的是腫瘤學經典綜述系列的最新版本“Hallmarks of Cancer”,總結了 14 種主要癌癥特征。

2000 年,麻省理工學院的 Robert A. Weinberg 教授和 Douglas Hanahan 教授在 Cell 雜志上聯合出版了第一版“The Hallmarks of Cancer”。文章發表后,一時洛陽紙貴,立即成為該領域的經典綜述,后來更是成為 Cell 雜志歷史上被引用次數最多的綜述之一(目前超過 37000 次)。

2011 年,兩位教授對最初的六大癌癥特征進行了更新和擴展,他們撰寫的“Hallmarks of cancer: the next generation”也跟上了時代的步伐,至今仍在 Cell 雜志上發表,目前已被引用超過57000次。

十年過去了,現在 2022 年第三版“Hallmarks of Cancer”已經正式發布,第三版是 Hanahan 教授獨作。據公開資料顯示,Robert A. Weinberg 教授今年即將年滿80歲,而 Hanahan 教授也已過古稀之年。祝愿兩位教授健康長壽,我們也倍加珍惜這部“十年凝一篇”的佳作。

第一版(2000 年):癌癥 6 大特征
“癌癥的 6 大特征”濃縮了過去一個世紀癌癥研究的內容,建立了理解癌癥不同表型的基本邏輯框架。腫瘤的發生和發展是漸進的、多步驟的。在將正常細胞轉化為腫瘤細胞的過程中,這些標志性功能逐漸獲得,并最終演變為惡性病變。

2000 版“癌癥的 6 大特征”分別是:
1.自給自足的生長信號:如 H-RAS 致癌基因的激活。
2.對生長抑制信號不敏感:例如,視網膜母細胞瘤(Rb)基因(腫瘤抑制基因)缺失。
3.逃避凋亡:如產生 IGF 因子。
4.無限的復制潛力:如激活端粒酶。
5.持續的血管生成:如 VEGF 誘導物的產生。
6.組織侵襲和轉移:如 E-鈣黏蛋白的失活。
第二版(2011年):癌癥 10 大特征
該版本在原有的 6 大特征的基礎上增加了 4 個新特征,即:細胞能量代謝的失控、逃避免疫清除、腫瘤促炎癥作用、基因組的不穩定性和突變,并對原有 6 個特征概念的內涵和外延進行了一些調整。
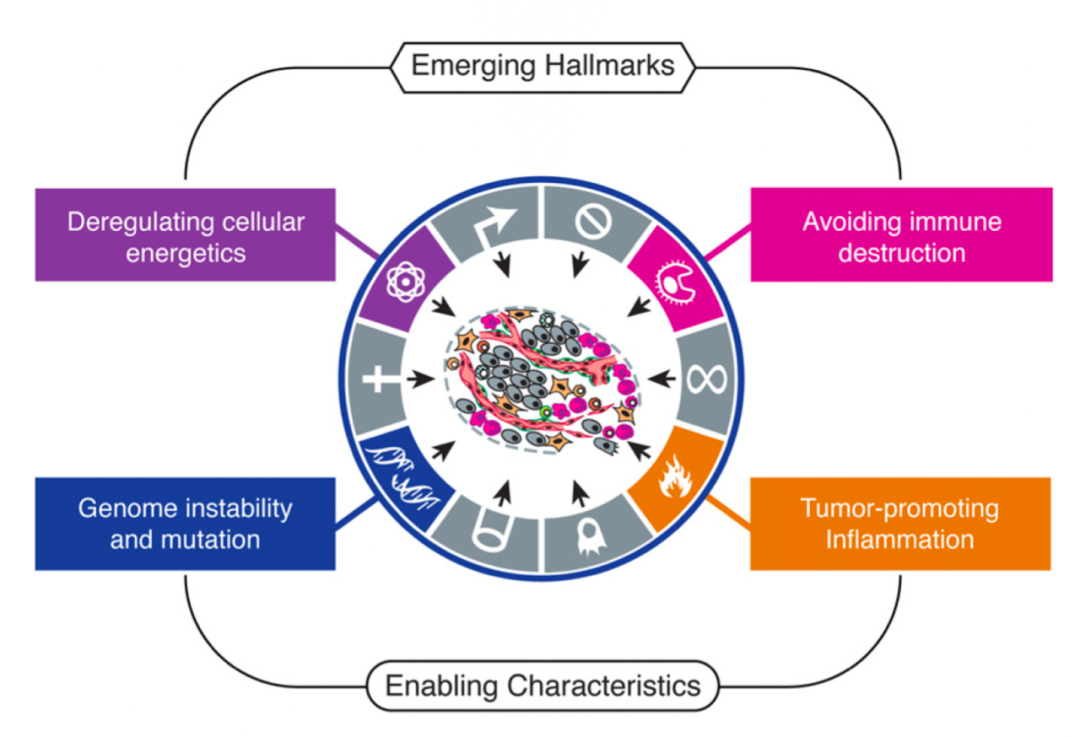
這 4 個新特征考慮了腫瘤代謝、腫瘤免疫和基因組不穩定性在腫瘤發生和發展中的重要作用。在新增的特征中,前兩個被定義為“初現特征”,尚未得到充分驗證;后兩者被定義為“賦能特征”,因為它們是腫瘤狀態異常的結果。此外,作者還明確指出,腫瘤的發展不僅僅是腫瘤細胞的增加,還需要圍繞“腫瘤微環境”來理解。
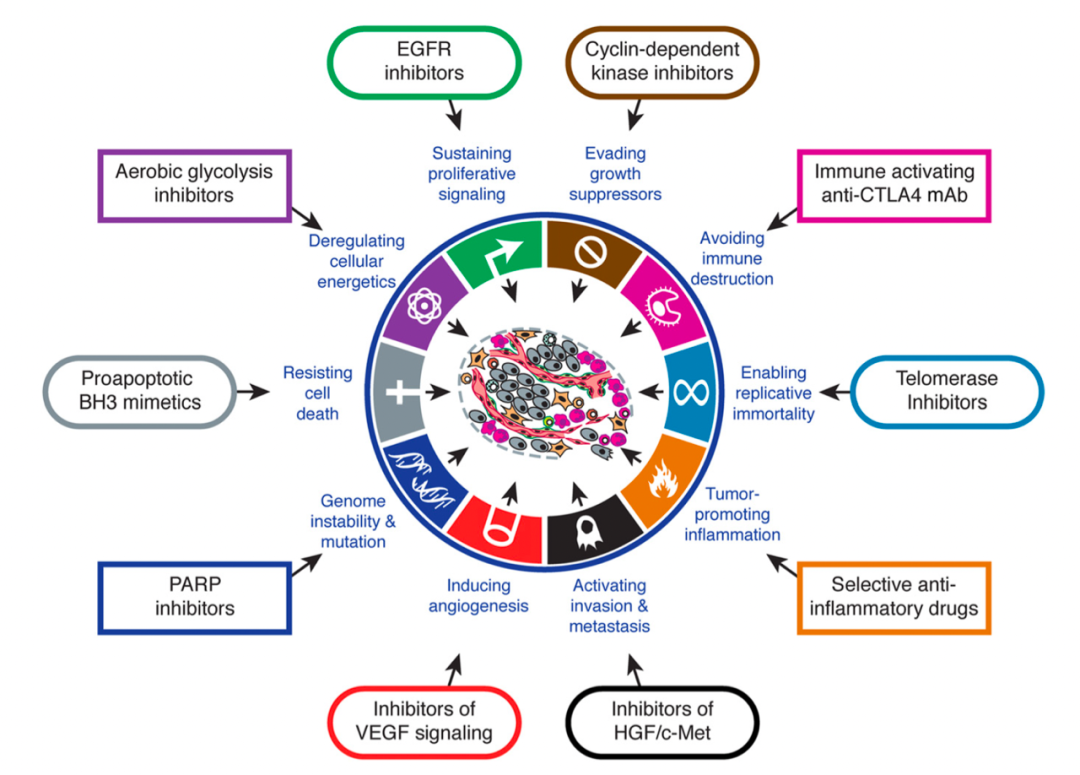
自上個世紀分子生物學發展以來,基礎研究與新藥開發密不可分。許多新藥的研發都是基于對腫瘤獨特的標志性分子事件的深刻理解,其直接靶向過程往往是一個關鍵節點(阿喀琉斯之踵,Achilles' Heel)。因此,作者以 10 種藥物為例,進一步佐證了“癌癥 10 大特征”所具有的實際意義。
1.“持續增殖信號”vs“EGFR 抑制劑”;
2.“避免生長抑制”vs“細胞周期依賴性激酶(CDK)抑制劑”;
3.“逃避免疫清除”vs“激活免疫的抗CTLA-4單克隆抗體”
4.“無限復制的能力”vs“端粒末端轉移酶抑制劑”;
5.“腫瘤促炎癥作用”vs“選擇性抗炎藥物”;
6.“激活浸潤和轉移”vs“HGF/c-Met 抑制劑”;
7.“促血管生成”vs “VEGF 抑制劑”;
8.“基因組的不穩定和突變”vs“PARP 抑制劑”;
9.“抵抗細胞死亡”vs“誘導凋亡的 BH3 類似物”;
10.“細胞能量代謝的失控”vs“有氧糖酵解抑制劑”。
第三版(2022 年):癌癥的 14 大特征
在原有 10 個特征的基礎上,增加了 4 個新特征,即解鎖表型可塑性、非突變表觀遺傳重編程、多態性的微生物組和衰老細胞。
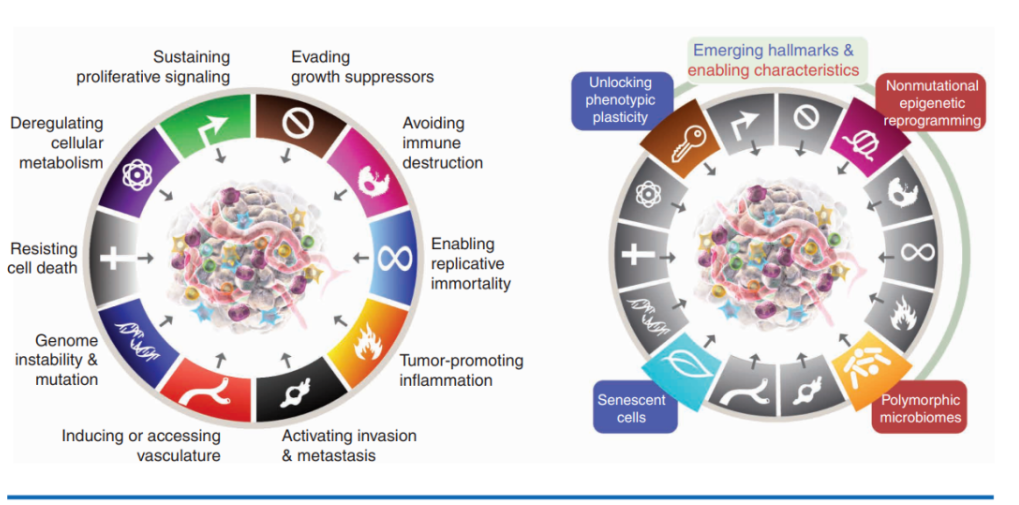
其中,表型可塑性和細胞衰老歸于初現特征,需要進一步更全面研究和驗證;表觀遺傳學重編程和微生物組多態性被定義為賦能特征,表明它們是腫瘤發展和獲得其他特征的驅動因素。
新增的 4 大特征的具體內容如下:
1.解鎖表型可塑性,而表型可塑性可以破壞細胞分化。作者將其分為三個方面:細胞去分化、細胞分化中斷和細胞轉分化。

2.非突變表觀遺傳學重編程:表觀遺傳是指 DNA 序列沒有變化,但基因功能有可遺傳的變化。它還包括三個方面:誘導表觀遺傳學重編程的環境機制、表觀遺傳學調控的異質性以及腫瘤微環境中基質細胞的表觀調控。
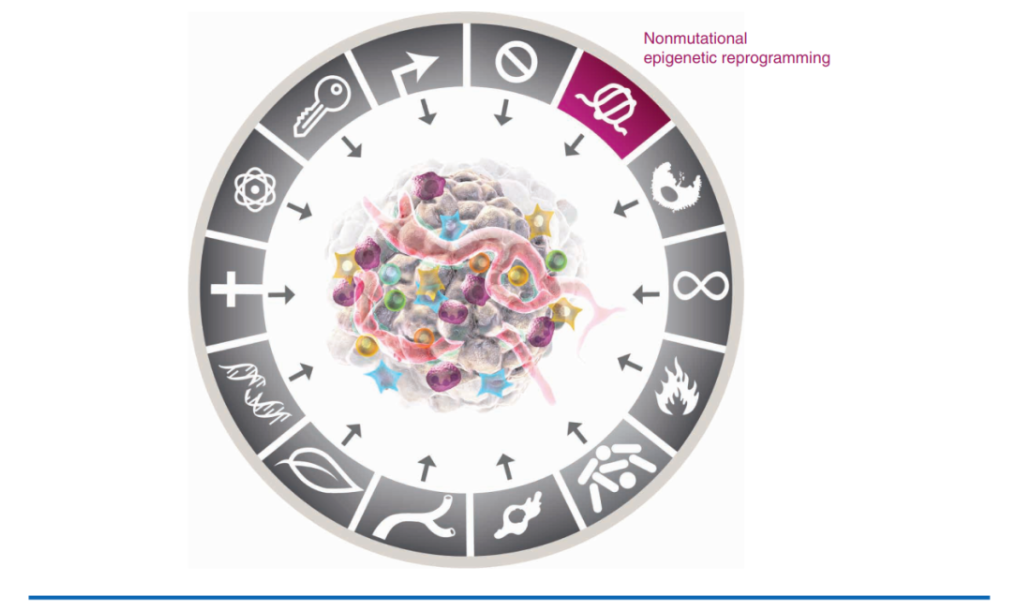
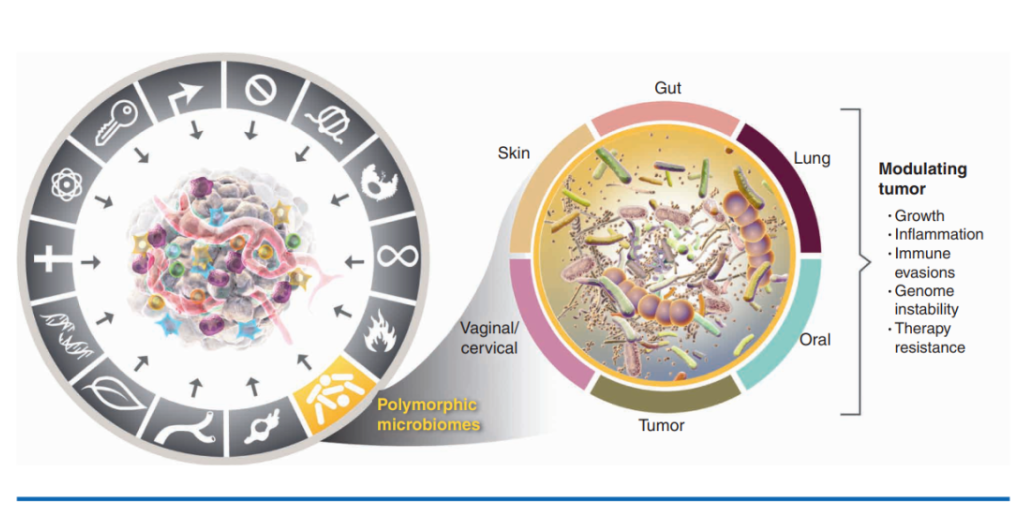
3.多態性的微生物組,大量存在于結腸、其他黏膜及其連接部位,或腫瘤內部的微生物群落構成腫瘤的微生物組。腫瘤微生物組具有極高的多態性,在腫瘤的發生、發展和治療響應中發揮著重要作用。
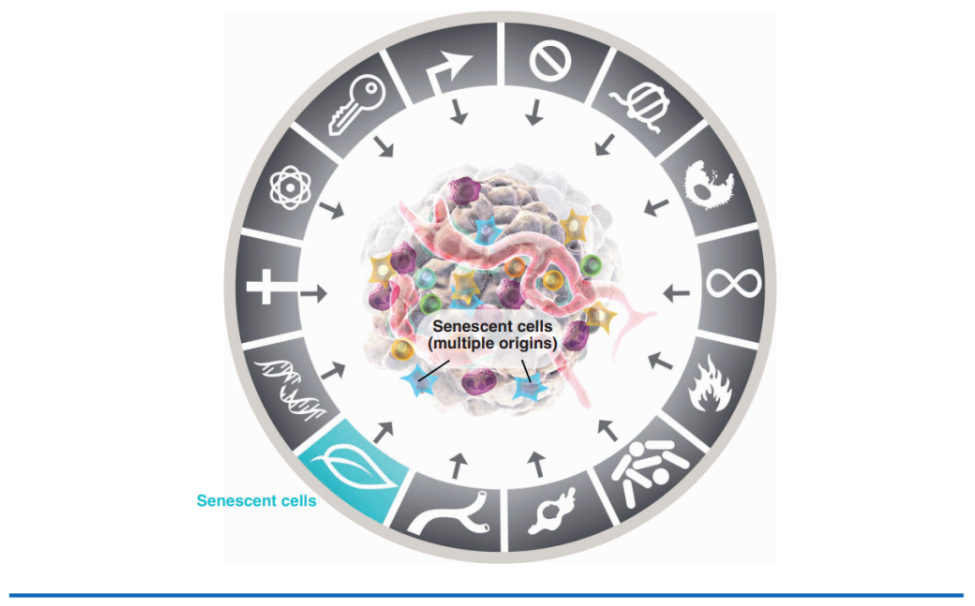
4.衰老細胞:細胞衰老通常被認為是一種不可逆轉的抑癌性保護機制,可以維持組織內部環境的穩定。然而,越來越多的證據表明,在某些情況下,衰老細胞可以通過衰老相關分泌表型(SASP)等方式促進腫瘤的發生和發展。然而,關于衰老作為腫瘤標志物的研究仍處于起步階段,需要進一步廣泛的驗證和嚴格的審查。
癌癥的概念化和特征化概括可以作為一種工具,將癌癥表型和基因型的復雜性濃縮為一個簡明的理論。隨著對癌癥發生和發展機制的深入了解,癌癥的多種特性也表現出概念化為特征的潛力。在這些新特征中,表型可塑性和分化中斷共同構成了一個獨立的特征,而非突變性的表觀遺傳重編程和多態微生物群落構成了獨特的、有助于其他的賦能特征。此外,來自不同來源的衰老細胞也可以被視為腫瘤微環境中具有重要功能的細胞類型,因此它們也被添加到“初現特征”中進行進一步研究。
癌癥的多樣性具有廣度和范圍,其多樣性表現跨越了遺傳學、細胞和組織生物學、病理學和治療響應特征。癌癥包含的各種疾病的多種表現形式都呈現出海量的“大數據”。對癌癥特征的綜合化概念將有助于逐步完善為一套科學理論。
免責聲明:
我們尊重原創,也注重分享。圖文來源網絡,版權歸原作者所有,如涉及作品內容、版權或其它問題,請聯系我們刪除!


 閩公網安備 35020602002648 號
閩公網安備 35020602002648 號 QQ 客服
QQ 客服
