神經系統疾病往往復雜且難以治愈,一直是醫學界的一大挑戰。近年來,干細胞技術的進步為這一領域注入了新的活力。

干細胞不僅具有修復和再生受損組織的能力,還可以調節人體免疫系統,從而在治療各種神經系統疾病方面顯示出顯著的優勢。這項技術有望成為治療神經系統疾病的新方法,為患者提供更有效的治療途徑。
對于人體來說,雖然大多數組織都有一定程度的自愈能力,但神經系統是不同的。
由于中樞神經系統(CNS)的再生能力有限,多發性硬化癥、帕金森病、脊髓損傷或創傷性腦損傷等神經損傷往往難以恢復,這些損傷的治療極具挑戰性。因此,神經系統疾病的治療選擇相對較少。
為了解決這個問題,科學家們致力于開發創新的治療方法,希望提高神經損傷相關疾病的治療效果,為患者帶來更多的希望和康復可能性。
近年來,基于干細胞的再生醫學逐漸成為治療此類疾病的有吸引力的方法。其中,間充質干細胞(MSCs)因其獨特的特性而成為最受青睞的細胞來源之一。多項研究表明,干細胞治療神經系統疾病的機制包括通過旁分泌作用提供神經營養和免疫調節,或通過受損細胞的再生和替代達到治療效果,這有望為此類疾病提供新的治療選擇。
01 全世界有數百萬人患有神經系統疾病,因為它們很難治愈!
神經系統是人體重要的調節系統之一,負責信息傳遞、運動控制和各種生理功能的協調。然而,由于遺傳因素、環境因素、創傷或其他不確定的原因,神經系統疾病的發生給患者及其家屬帶來了巨大的痛苦。
神經系統疾病的范圍很廣,主要包括神經退行性疾病、神經傳導障礙和神經炎癥。具體來說,神經系統疾病可分為以下幾類:
神經血管疾病,如腦梗死、腦出血和短暫性腦缺血發作。
中樞神經系統傳染病:包括腦炎、腦膜炎和脊髓炎。
神經退行性疾病:常見的包括阿爾茨海默病、帕金森病等。神經創傷:如硬膜下血腫和創傷性腦損傷。
腫瘤:包括神經系統的原發性腫瘤,如膠質瘤和顱內轉移瘤。脫髓鞘疾病:如多發性硬化癥和視神經炎。
代謝和營養紊亂:如維生素 B1 缺乏引起的多發性神經病變或維生素 B12 缺乏引起的亞急性聯合變性。
其他:包括中毒和威爾遜氏病等遺傳性疾病。
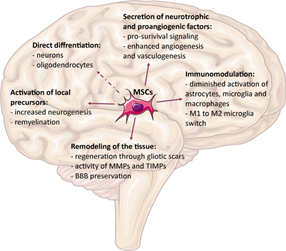
盡管這些神經系統疾病的類型不同,但它們引起的主要癥狀大多相似,如意識障礙、運動障礙、語言和言語障礙、認知功能障礙和情緒障礙。
從病因的角度來看,神經系統疾病大致可分為三種主要類型:
與特定腦區神經元喪失有關的疾病,如帕金森病(PD)和多發性硬化癥(MS)。
急性損傷引起的神經元喪失性疾病,如中風。
與細胞功能障礙有關的疾病,如癲癇。
大腦發育異常的原因通常是多方面的,包括衰老、環境因素、長期壓力、創傷性腦損傷和基因突變。例如,淀粉樣前體蛋白(APP)、早老素-1 和早老素-2 的基因突變,或載脂蛋白 E(ApoE)突變與神經退行性疾病的發展密切相關。
目前,神經系統疾病已成為現代醫學面臨的主要挑戰之一。由于治療困難,許多患者在診斷后很難獲得有效和標準化的治療計劃,使這些疾病成為全球第二大死因,給無數家庭帶來了沉重的經濟和心理負擔。
隨著時間的推移,科學界的持續研究加深了我們對神經系統疾病的理解,并推動了治療方法的創新。越來越多的研究致力于揭示其發病機制,尋求新的治療方法來提高患者的生活質量。
02 干細胞在神經系統疾病治療中的臨床應用
在眾多治療方法中,干細胞因其自我更新和多向分化能力而成為神經再生和修復的理想細胞來源。近年來,臨床研究表明,干細胞已成為治療難治性神經系統疾病的一種非常有前景的治療選擇。
在神經系統疾病的治療中,干細胞主要通過以下機制發揮作用:
修復損傷:干細胞可以遷移到受損的神經部位,通過細胞置換替換死亡或受損的神經細胞,修復受損的神經網絡。
細胞遷移:在體內組織損傷后,間充質干細胞(MSCs)可以選擇性地遷移到受損的組織或器官微環境中,以維持或重塑其細胞功能。這一過程涉及多種細胞因子和細胞信號通路的參與。
細胞分化:干細胞可以分泌大量的活性生長因子和營養因子,激活神經細胞,促進新細胞的再生和重建;同時分泌血管生成因子以促進受影響區域的血管生成。
免疫調節:干細胞可以抑制 T 細胞增殖,調節 Th2/Th1 細胞比例,阻斷 B 細胞的細胞周期,抑制細胞增殖和抗體產生,從而發揮抗炎保護作用。
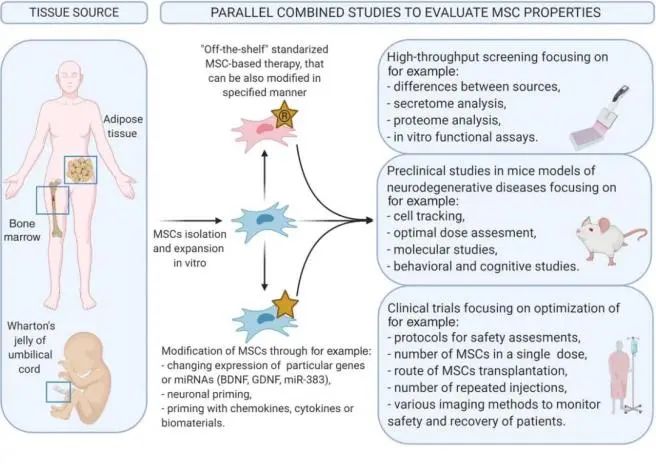
間充質干細胞已在 200 多項臨床研究中注冊,這些研究使用各種干細胞方法治療神經系統疾病,涵蓋了多發性硬化癥、中風、帕金森病和脊髓損傷等主要疾病。以下是近年來干細胞在一些常見神經系統疾病中的臨床療效。
1. 干細胞與中風(CVA)
中風可導致神經元損傷。對干細胞轉運 MED 的研究表明,干細胞可以再生和修復受損的腦神經元,從而減少中風患者的后遺癥癥狀。在 9 名不同年齡的腦卒中偏癱患者中,將干細胞移植到腦梗塞區域取得了顯著的臨床效果。

9 名患者的成像顯示病變區域的組織發生了顯著變化。影像學顯示,移植到腦梗死病變中的干細胞分化為神經系統的各種細胞,分泌營養因子,促進神經和血管再生,修復受損的血腦液屏障,減少炎癥反應,促進腦梗死動物神經功能的恢復。結果,9 名臨床患者的偏癱癥狀明顯改善。
干細胞通過利用旁分泌功能、分泌血管內皮生長因子(VEGF)、促進腦血管生成、重塑血管、恢復內皮完整性、降低通透性和減少細胞凋亡,在重塑血管和維持中風血流方面發揮著重要作用。

研究證實,干細胞可以在中風后重塑血管并維持腦血流。
2. 干細胞和阿爾茨海默病(AD)
干細胞也為阿爾茨海默病和帕金森病等神經退行性疾病患者帶來了新的治療選擇。Advanced Science 的一篇文章表明,臍帶間充質干細胞(hUC-MSCs)具有修復受損神經細胞的功能,可以通過 HGF-cMet-AKT-GSK3β 途徑調節 tau 蛋白磷酸化,顯著改善阿爾茨海默病模型動物的學習、記憶和認知能力。

HGF 介導的臨床級人臍帶間充質干細胞改善了加速衰老阿爾茨海默病小鼠模型的功能恢復。
許多臨床試驗也表明,干細胞移植治療阿爾茨海默病不僅可以調節大腦中的炎癥環境,還可以促進神經再生和突觸連接,有效改善疾病,并且安全無副作用。
3. 干細胞和帕金森病(PD)
帕金森病是一種進行性神經退行性疾病,主要見于 60 歲以上的人,其特征是大腦多個區域的特定腦細胞(神經元)死亡。干細胞療法在治療帕金森病方面取得了新的突破。為了提高細胞移植后的低存活率,哈佛醫學院將調節性 T 細胞和 iPSC 衍生的中腦多巴胺神經元(mDAN)移植到動物模型中。結果表明,mDANs 的存活率顯著提高,動物行為迅速恢復,為帕金森病的治療提供了一種新的可能選擇。

除了自體 Treg 細胞聯合細胞移植治療帕金森病外,針對帕金森病的干細胞療法也取得了令人鼓舞的結果。2023 年 8 月,拜耳宣布其治療帕金森病的干細胞藥物 BRT-DA01 已達到第一階段試驗的終點,并為患者帶來了令人驚訝的結果。12 名受試者被分為高劑量組和低劑量組,在接受 BRT-DA01 治療的一年內沒有發生不良事件。
根據帕金森病綜合評價量表 MDS-UPDRS 第三部分(運動功能檢查)和運動功能狀態評估工具 Hauser Diary,所有受試者的次要探索性臨床終點均有改善,高劑量組的改善更為顯著。
據報道,BRT-DA01 的 II 期臨床試驗目前正在計劃中,預計將于 2024 年上半年開始招募患者。帕金森病患者可能有新的治療希望。
4. 干細胞與肌萎縮側索硬化癥(ALS)
面對退行性疾病,人類幾乎無能為力,但干細胞技術的出現給這些疾病帶來了新的希望。肌萎縮側索硬化癥(ALS),俗稱“ALS”,是一種幾乎無法治愈的罕見疾病,但 iPSC 干細胞技術的出現似乎給它帶來了一線希望。
JNeurosci 上的研究顯示,科學家們使用 iPSC 技術在 ALS 患者中發現了一種可能的遺傳變異,這甚至可能成為治療該疾病的新靶點。這項研究為 ALS 的治療帶來了新的希望。

ALS 患者的 SYNGAP1 3'UTR 突變通過 HNRNPK 的募集導致 SYNGAP1 剪接異常和樹突棘丟失。在另一名接受 MSCs 治療的 ALS 患者中進行的一項臨床研究表明,與實驗動物一樣,患者的疾病進展速度減慢。
病例對照研究涉及 67 名接受沃頓神經膠質干細胞(WJ MSCs)治療的 ALS 患者。所有患者均接受了三次沃頓粘合劑(WJ)-MSC 的 IT 輸注。在整個研究人群中,31% 的患者觀察到疾病進展放緩。對 WJ-MSC 治療的早期反應可以預測 ALS 患者的預后和延長生存期。

5. 干細胞與多發性硬化癥(MS)
MS 長期以來被稱為“不死的癌癥”,其嚴重程度是顯而易見的。干細胞作為一種新興療法,正逐漸成為患者的新希望。在靈長類動物 MS 模型中 MSC 治療的一項研究中,發現鞘內輸注 MSC 可以延緩 EAE 猴的神經功能障礙和神經元脫髓鞘。
臨床研究表明,IT 或 IVMSC 移植過程對患者來說是可行、安全和可耐受的。通過擴展殘疾狀態量表(EDSS)評估,一些患者表現出臨床穩定或改善的跡象。
在瑞典,對 7 名多發性硬化癥患者進行了一項 I 期臨床研究。結果顯示,在臨床緩解期間接受自體骨髓間充質干細胞移植的患者中,86% 達到了穩定的殘疾狀態。輸注后一周內檢測到外周血中調節性 T 淋巴細胞比例的增加,表明 MSC 在 MS 患者中具有免疫耐受性。該研究還提出分析接受 MSC 治療的 MS 患者的主要結果,以使用 MRI 探索組織的微觀完整性。

6. 干細胞與脊髓小腦失調癥(SCA)
脊髓小腦障礙(SCA)是一種難以治愈的神經退行性疾病。該研究評估了靜脈注射和鞘內注射人臍帶間充質干細胞(MSCs)治療 SCA 的安全性和可行性。
結果顯示,在治療后的 12 個月隨訪期間,沒有發生嚴重的移植不良事件,SCA 癥狀得到緩解。這為人臍帶間充質干細胞移植治療 SCA 和其他遺傳性神經疾病提供了一種新策略。
7. 干細胞與創傷性腦損傷 (TBI)
當頭部突然受到猛烈撞擊或搖晃時,可能會發生創傷性腦損傷(TBI),腦震蕩是最常見的TBI 類型。
由于神經可塑性,創傷性腦損傷的干細胞療法可以通過在整個生命過程中形成新的神經連接來刺激神經元自我重組。這種方法不僅可以產生新的細胞,還可以增強現有的神經可塑性。
中國神經修復學會(籌備委員會;CANR)和國際神經修復學會中國委員會(IANR)正式發布了《顱腦創傷臨床神經修復治療指南2022版》。該指南明確指出,細胞治療的臨床試驗被視為中重度創傷性腦損傷的I級證據,這有助于提高基于細胞治療的神經損傷修復的有效性,并在促進創傷性腦損傷基礎和臨床研究方面發揮重要指導作用。

此外,國際期刊 International Journal of Oral Science 的一篇文章詳細介紹了干細胞治療 TBI 的潛在分子機制,證明了其緩解神經炎癥、修復腦損傷的能力,并為 TBI 和其他神經系統疾病的臨床干預提供了新的治療靶點。

研究表明,SHED EVs/miR-330-5p 靶向小膠質細胞極化中 Ehmt2-H3K9me2 介導的 CXCL14 轉錄變化,用于治療創傷性腦損傷。
人類有許多類型的神經系統疾病很難治愈,甚至無法治愈。干細胞具有組織再生和免疫調節的作用,是一種不同于傳統醫學的創新療法。通過在人類細胞基因水平上解決疾病問題,它們在治療許多疾病方面顯示出廣闊的前景。
隨著再生醫學技術的不斷進步,在進展緩慢的難治性和難治性疾病方面取得了新的突破。干細胞有望為治療更多神經系統疾病帶來新的選擇。
免責聲明:我們尊重原創,也注重分享。圖文來源網絡,版權歸原作者所有,如涉及作品內容、版權或其它問題,請聯系我們刪除!


 閩公網安備 35020602002648 號
閩公網安備 35020602002648 號 QQ 客服
QQ 客服
