目前,家家戶戶幾乎都進入了“應陽盡陽”模式,周圍的家人、朋友也已經紛紛"陽康",慢慢回歸正常生活。然而,有一種非常普遍的情況——即使在轉陰后,身體仍然虛弱,腳步輕浮,容易疲勞。
事實上,除了感染新冠病毒時的一系列疾病反應外,我們更擔心的是陽后的疲勞和其他疾病會持續多久?換句話說,是新冠后遺癥。

01 長新冠,究竟是什么?
新冠后遺癥更為準確的說法應該是“新冠急性后遺癥”“新冠后癥狀”“慢性新冠綜合征”,或者稱“長期新冠肺炎(Long Covid)”。
現階段,世界衛生組織(WHO)對“長新冠”的定義為:在新冠感染后 3 個月仍存在癥狀,至少持續 2 個月,且無法用其他診斷來解釋;最為常見的是疲勞、呼吸急促和睡眠障礙或失眠。
因此,大多數陽康都經歷過干咳、疲勞、呼吸急促等經歷,還不能稱之為長新冠肺炎,只是正常的恢復期(甚至是在感染后的急性期)。
當然,長新冠確實是存在的,但影響究竟有多大?
02 長新冠,占比有多少?
醫學頂刊 JAMA 曾回答過這個問題。這項研究由 WHO 牽頭以及全球各地的科學家合作完成,匯集了 54 項研究和 2 個醫療數據庫,涵蓋了 120 萬名新冠感染者的數據。
結果顯示:在感染新冠的 3 個月后,有 6.2% 仍存在至少一種癥狀;到感染的 1 年后,有 0.9% 還在經歷新冠后遺癥。
常見的長新冠肺炎癥狀有三種:約 3.2% 的持續疲勞,并伴有身體疼痛或情緒變化;3.7% 的持續呼吸道問題,主要癥狀為呼吸困難和持續咳嗽;還有 2.2% 的認知問題,健忘或注意力無法集中,即最近經常聽到的腦霧。
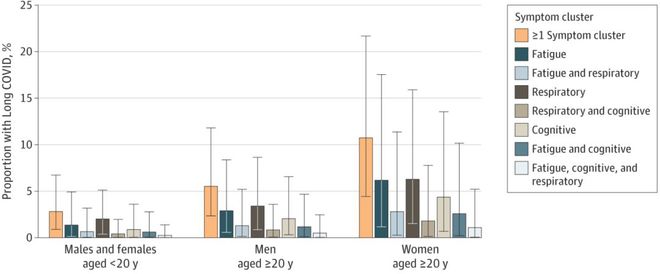
▲ 長新冠比例
這項基于早期毒株的數據顯示,有 6.2% 的新冠感染者會經歷長新冠;而在奧密克戎感染潮中,長新冠的幾率會降低 0.24-0.50(取決于上一針疫苗的接種時間)。
6.2%,即使是奧密克戎,也有 3% 的概率,約 1-4.7%,不高但不低。根據本研究中的 120 萬陽性,有 3.7-5.6 萬陽康將有一個長新冠,特別是在今天的新冠病毒感染者數量如此之多,每個人似乎都在打開盲盒,無法預測感染三個月后是否會發生。
然而,柳葉刀子刊 eClinicalMedicine 于 12 月 1 日發表了一篇針對長新冠的系統評價和 Meta 分析,涵蓋 194 項研究和 735,006 名參與者,披露了個“駭人聽聞”的數據:
無論是否住過院,在隨訪的 4 個月內(平均 126 天),至少 45% 的新冠感染者仍存在一種及以上的癥狀;最普遍的五個癥狀分別是疲勞(28.4%)、疼痛/不適(27.9%)、睡眠障礙(23.5%)、呼吸困難(22.6%)和活動受限(22.3%)。
即使在非住院的人群中,最常見的長新冠癥狀依舊是疲勞,該比例高達 34.8%!
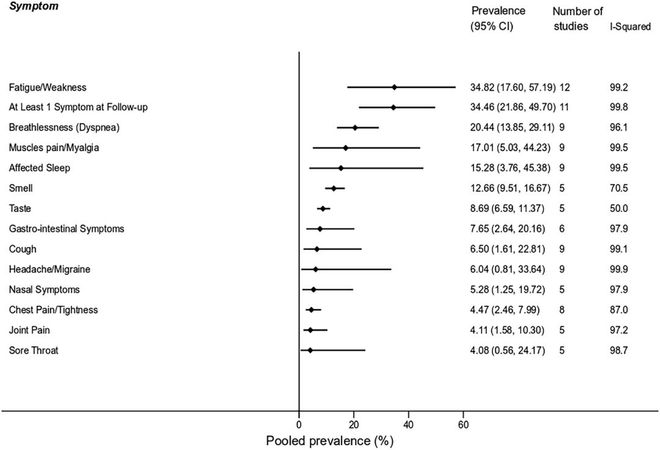
▲非住院人群中長新冠各癥狀的比例
以上兩篇綜述也提醒我們,長新冠不容忽視,尤其是持續的身體疲勞。
03 長新冠,背后的機制?
以上研究均為基于大樣本人群的調查,近日來自維也納大學的研究團隊發現了感染新冠病毒后觸發長新冠之疲勞綜合征的病理機制——過度的抗炎反應。
不同于經典的免疫炎癥反應,在新冠病毒的侵略下,長新冠患者的體內出現了另一種抗炎模式,即交替極化巨噬細胞的主導疾病模式,直接誘發了長期疲勞綜合征的發生。該研究于 12 月 2 日發表在 Cell子刊iScience 上。

在本研究中,研究員招募了三組參與者,每組 13 人,年齡和性別匹配:
1. 新冠病毒疫苗完全注射后至少三個月,未感染新冠病毒;
2. 至少三個月前感染新冠病毒,但入組時完全恢復,無癥狀;
3. 感染新冠病毒后至少三個月仍有疲勞,即長新冠患者(LCS)。
免疫激活標志物分析顯示,LCS 組中既沒有觀察到上調的促炎細胞因子,也沒有細胞因子的升高,甚至降到了相當低的水平。即,長新冠患者體內缺乏促炎活動和全身炎癥。
本研究的首席作者 Christopher Gerner 表示,與健康組相比,LCS 患者體內檢測到的急性炎癥的關鍵標志處于較低水平,或根本無法檢測到。換句話說,長新患者經歷的不是傳統的炎癥現象。新冠肺炎引起的長期疲勞不是炎癥,而是一種受影響的抗炎過程。
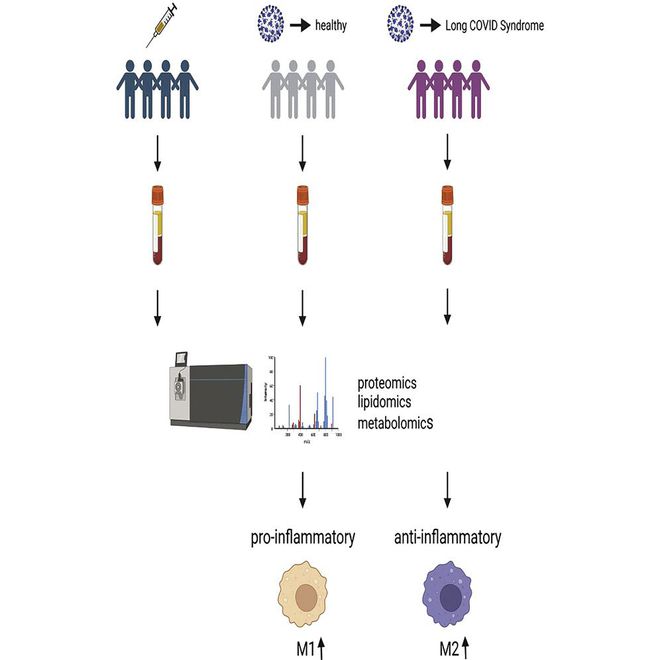
▲研究試驗過程
那么,在新冠病毒的不斷攻擊下,LCS 患者體內究竟發生了怎樣的變化,誘發了慢性疲勞綜合征呢?
與健康對照組相比,學者進一步利用脂肪酸和氧化脂質分析找到了端倪,LCS 該組的血漿中含有較高水平的抗炎氧化脂。還有各種抗炎蛋白和代謝物。
而這一系列明顯的炎癥抑制分子特征,讓研究者不得不想到了:在長新冠的患者體內,形成了交替極化的巨噬細胞。
人體中的巨噬細胞分為兩類,經典活化的 M1 型巨噬細胞和選擇性活化的 M2 型巨噬細胞。在新冠病毒的攻擊下,常見的經典促炎性 M1 細胞轉變為耐受性的 M2 細胞,導致抗炎模式的改變。
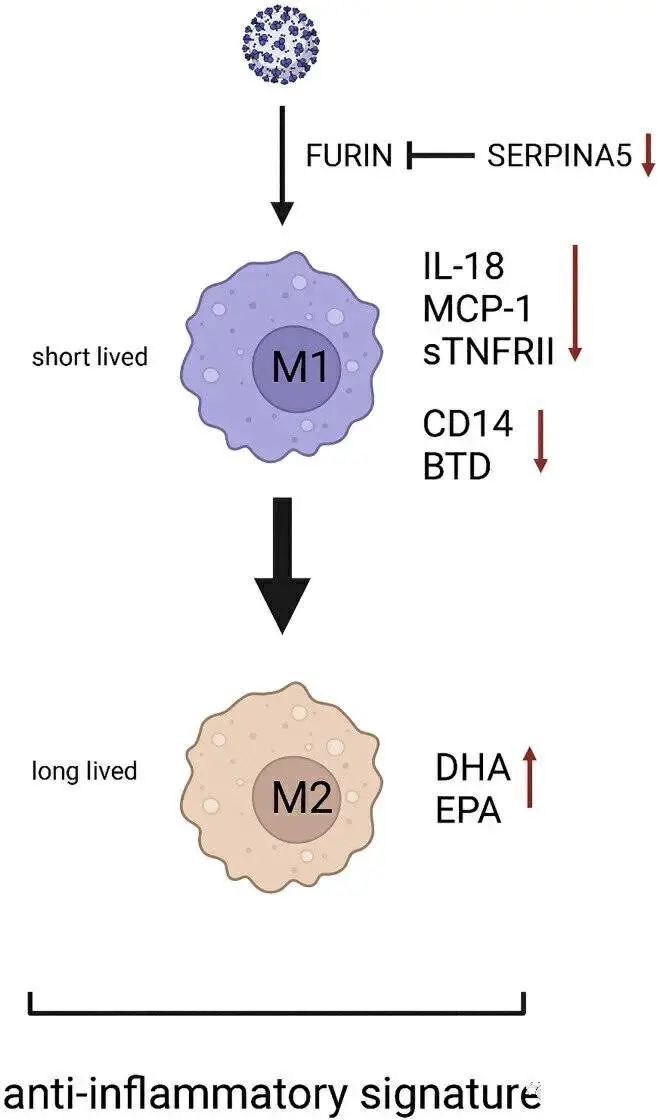
▲病理機制
正是在這種變化后的抗炎模式下,越來越多的抗炎模式 M1 型轉為 M2 型,牛磺酸和刺桐堿的抗炎滲入物水平上升,但氨基酸和甘油三酯水平下降,酰基肉堿失衡。而刺桐堿是一種能自發誘導睡眠的化合物,體內水平越大,自然越容易疲勞,直接引起長新冠的疲勞綜合征。
研究者表示,了解長新冠的病理學機制只是第一步罷了,希望在不久的將來,可以為這些“困于”長新冠的患者提供更多改善和治療的手段!
04 干細胞治療新冠后遺癥
針對新冠病毒對患者多臟器的傷害,全球醫療專家團隊一直在努力探索更有效的康復方式,而有帶著“修復”“再生”光環的干細胞為人類修復感染新冠病毒患者臟器損傷創造了可能。
(1)干細胞抗新冠的優勢
干細胞有一個非常顯著的特性——免疫調節特性,可以調節如抗原提呈細胞、T 細胞、B 細胞和自然殺傷 NK 細胞等重要免疫細胞的免疫功能。
間充質干細胞(MSC,mesenchymal stem cells)是干細胞家族的重要成員,其對免疫系統的調節特性具有雙向性,在免疫力低下時候,起到增強免疫的作用;而對過強的免疫反應,會產生抑制作用。
間充質干細胞(MSC)憑借其強的免疫調節特性,在這次疫情的治療中也發揮了重要作用。
(2)干細胞干預新冠的作用機制
間充質干細胞技術主要依賴于其自我更新能力、多潛能分化、低免疫原性、抗炎功能以及對受損組織的歸巢能力。此外,間充質干細胞具有獨特的免疫調節機制來調節先天和獲得性免疫反應。
間充質干細胞在干預新冠肺炎的研究中已經展示出積極信號,實驗表明,其主要通過以下幾方面的機制來發揮作用:
1)MSC 歸巢到損傷肺組織局部:研究認為,MSC 的歸巢機制可能與其表達一定的趨化因子受體有關。這些趨化因子受體與肺損傷時產生的趨化因子、細胞粘附分子和細胞因子共同作用,使干細胞向損傷部位募集以發揮最大效應。
2)MSC 可分化為損傷肺組織:多數早期 MSC 治療機制的研究都基于其多向分化性,一些研究也證實 MSC 在肺內可以分化為肺內細胞。如 Rojas 等發現骨髓 MSC 在博萊霉素誘導的肺損傷模型中可以分化為肺泡 Ⅰ 型、Ⅱ 型上皮細胞、成纖維細胞、肌成纖維細胞。
3)MSC 可調節炎癥反應:MSC 不僅能多向分化,而且具有特殊的免疫調節功能,這使其在 ARDS 中能起到調節炎癥反應的作用。MSC 具有一定免疫調節特性,能抑制 T 淋巴細胞的激活和增殖,以及抗原提呈細胞、NK 細胞和 B 細胞的活性。炎癥反應時,MSC 能改變細胞因子的效應模式,使 Th1 細胞為主的促炎性反應轉變成 Th2 細胞為主的抗炎性反應。
可見,MSC 具有免疫抑制功能,可抑制炎性反應,增強抗炎作用,以恢復器官功能和促進修復的損傷,疾病早期使用更有助于發揮其抗炎作用。
4)MSC能減輕肺部液體滲出:多項研究證明,MSC 可以減輕肺的液體滲出,這一方面與 MSC 能恢復或增強肺泡液體清除能力有關;另一方面是因為 MSC 能促進受損血管內皮細胞和肺泡上皮細胞的修復,維持肺血管屏障的完整性,改善其通透性。
a. MSC 可增加肺泡液體清除能力:肺泡液體清除(AFC)受損可能導致 ARDS 患者的發病率和病死率增加。
b. MSC 有助于維持肺泡血管屏障的完整性:以往認為 MSC 維持肺泡血管屏障的完整性和穩定性與干細胞的植入和轉分化有關,MSC 在肺損傷局部旁分泌產生的各種可溶因子間接促進了肺的修復。
新冠肺炎疫情爆發至今,科學家們眾志成城,共同探尋有效的治療方法,間充質干細胞已經成為了全球抗疫的“秘密武器”。目前,國內外已完成多項干細胞用于 COVID-19 患者的臨床研究,超過 10 項研究結果已發表。
臨床上正在繼續探索新冠后遺癥的機制,深入了解新冠后遺癥的成因,開展多種新冠后遺癥的療法探索,干細胞療法從新冠研究延伸至干預長期新冠癥狀的研究,在全球科學家的共同努力下,相信干細胞療法將為飽受新冠后遺癥折磨的患者帶來康復的希望。
免責聲明:
我們尊重原創,也注重分享。圖文來源網絡,版權歸原作者所有,如涉及作品內容、版權或其它問題,請聯系我們刪除!


 閩公網安備 35020602002648 號
閩公網安備 35020602002648 號 QQ 客服
QQ 客服
