2024 年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)的揭曉,如同夜空中綻放的璀璨煙火,照亮了生命科學(xué)的浩瀚天際。今年,這一至高榮譽(yù)被授予了兩位杰出的科學(xué)家——miRNA 的發(fā)現(xiàn)者,他們的成就為細(xì)胞治療鋪平了道路,開啟了生命科學(xué)的嶄新篇章。

諾獎(jiǎng)之光,璀璨綻放
2024 年的諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)授予了維克托·安布羅斯(Victor Ambros)與加里·魯夫昆(Gary Ruvkun)。這兩位研究者的貢獻(xiàn)是發(fā)現(xiàn)了微小 RNA(microRNA),并確定了這種分子在基因表達(dá)調(diào)控中起到的重要作用。

miRNA,即微小 RNA,這個(gè)曾經(jīng)鮮為人知的分子,如今成為了生命科學(xué)領(lǐng)域的明星。兩位獲獎(jiǎng)?wù)叩陌l(fā)現(xiàn),如同打開了一扇通往生命奧秘深處的大門,讓我們得以窺探細(xì)胞世界的奇妙運(yùn)作。
探索 microRNA 與基因調(diào)控
我們體內(nèi)的每個(gè)細(xì)胞都包含相同的遺傳信息,就像一本完整的手冊。那么,為什么肌肉細(xì)胞和神經(jīng)細(xì)胞如此不同呢?答案在于基因調(diào)控。通過精確控制基因的打開和關(guān)閉,每種細(xì)胞類型都可以選擇性地使用適合它們的“說明書”。
安布羅斯和魯夫昆對不同細(xì)胞類型如何發(fā)育產(chǎn)生了濃厚的興趣。他們研究了一種名為秀麗隱桿線蟲的小生物。盡管這種線蟲只有 1 毫米長,但它擁有許多類似于更復(fù)雜動(dòng)物的特殊細(xì)胞類型,使其成為研究多細(xì)胞生物組織發(fā)育的有用模型。
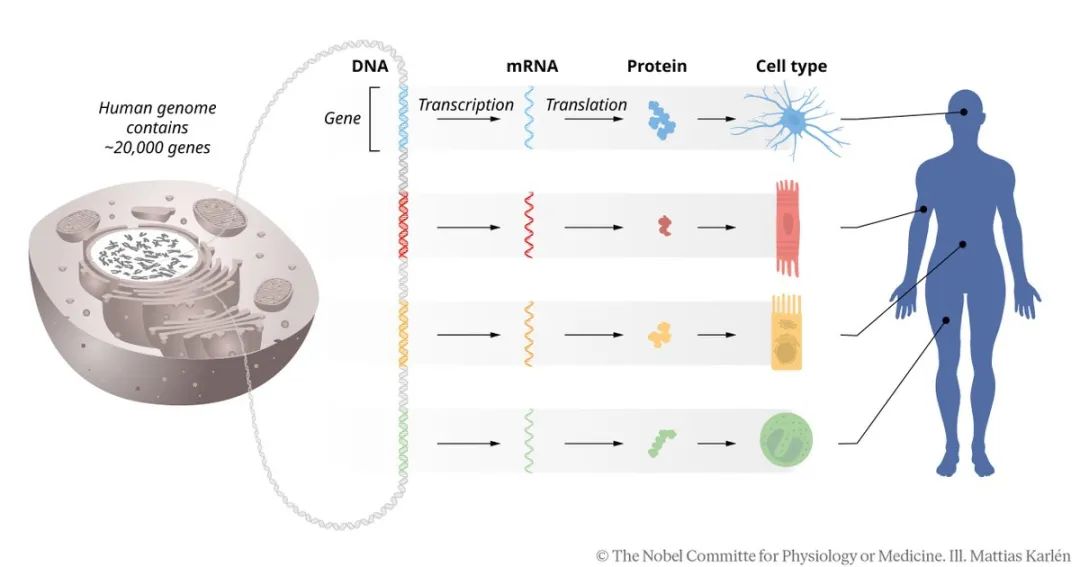
注:遺傳信息從 DNA 到 mRNA 再到蛋白質(zhì)的流動(dòng)。我們體內(nèi)所有細(xì)胞的 DNA 中都儲(chǔ)存著相同的遺傳信息。這需要精確調(diào)節(jié)基因活性,以便每種特定細(xì)胞類型中只有正確的基因組合具有活性。
兩位科學(xué)家分別研究了兩種線蟲突變株 lin-4 和 lin-14。這些突變株在發(fā)育過程中表現(xiàn)出異常的基因激活時(shí)間。安布羅斯發(fā)現(xiàn),lin-4 基因似乎是 lin-14 基因的負(fù)調(diào)控因子,但具體機(jī)制尚不清楚。
安布羅斯和魯夫昆在各自的實(shí)驗(yàn)室進(jìn)行了深入的研究。安布羅斯發(fā)現(xiàn) lin-4 基因產(chǎn)生一種不編碼蛋白質(zhì)的異常短的 RNA 分子。同時(shí),Lufkun 發(fā)現(xiàn) lin-14 基因的調(diào)控發(fā)生在蛋白質(zhì)合成階段,而不是 mRNA 生成階段。
當(dāng)兩位科學(xué)家比較他們的研究結(jié)果時(shí),他們驚訝地發(fā)現(xiàn) lin-4 的短序列與 lin-14 mRNA 的一段序列互補(bǔ)。進(jìn)一步的實(shí)驗(yàn)證實(shí),lin-4 mRNA 通過與 lin-14 mRNA 的互補(bǔ)序列結(jié)合來抑制 lin-14 蛋白的合成。
這一發(fā)現(xiàn)揭示了一種新的基因調(diào)控原理,由一種以前未知的RNA實(shí)現(xiàn)——微小RNA!
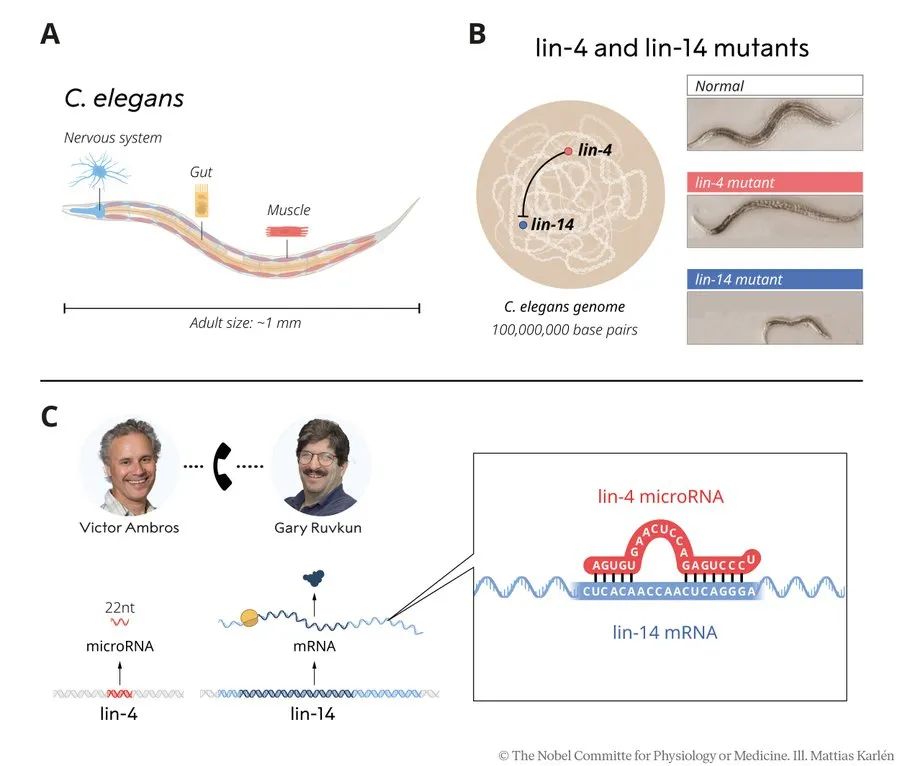
注:(A) 線蟲是了解不同細(xì)胞類型如何發(fā)育的有用模式生物。(B) Ambros 和 Ruvkun 研究了 lin-4 和 lin-14 突變。Ambros 證明 lin-4 似乎是 lin-14 的負(fù)調(diào)控因子。(C) Ambros 發(fā)現(xiàn) lin-4 基因編碼一種微小的 RNA,即 microRNA,它不編碼蛋白質(zhì)。Ruvkun 克隆了 lin-14 基因,兩位科學(xué)家意識(shí)到 lin-4 microRNA 序列與 lin-14 mRNA 中的互補(bǔ)序列相匹配。
起初,這一發(fā)現(xiàn)并沒有在科學(xué)界引起太大反響。許多人認(rèn)為,這可能只是線蟲的一種特殊現(xiàn)象,與人類無關(guān)。然而,在 2000 年,Lufkun 的研究小組發(fā)現(xiàn)了由 let-7 基因編碼的另一種微小 RNA。與 lin-4 不同,let-7 基因在整個(gè)動(dòng)物界高度保守。這一發(fā)現(xiàn)引起了科學(xué)界的極大興趣。
如今,我們知道人類基因組編碼 1000 多種微小 RNA,由微小 RNA 介導(dǎo)的基因調(diào)控在多細(xì)胞生物中無處不在。一個(gè)微小 RNA 可以調(diào)節(jié)多個(gè)不同基因的表達(dá),相反,一個(gè)基因也可能受到多個(gè)微小 RNA 的調(diào)節(jié),從而協(xié)調(diào)和微調(diào)整個(gè)基因網(wǎng)絡(luò)。
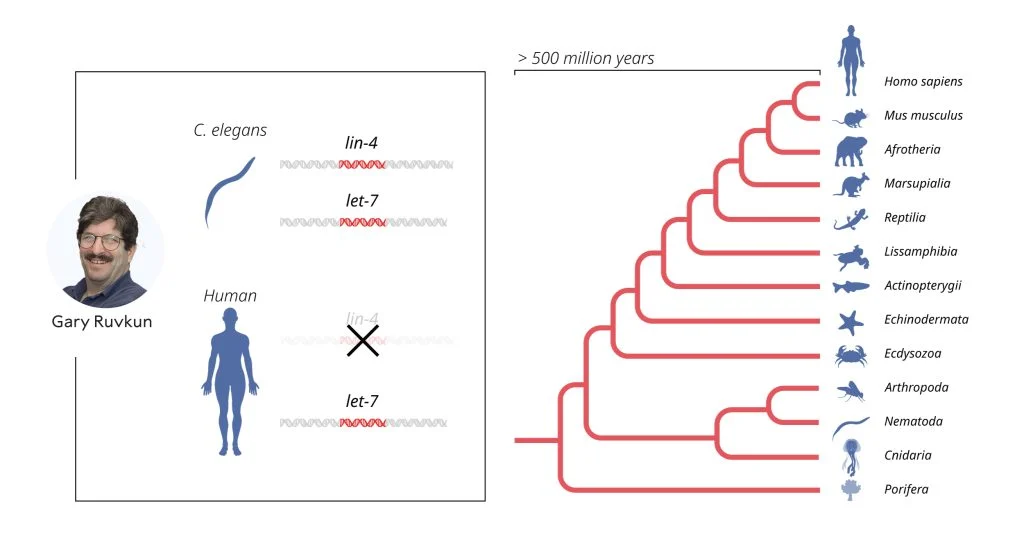
注:Ruvkun 克隆了 let-7,這是編碼 microRNA 的第二個(gè)基因。該基因在進(jìn)化中是保守的,現(xiàn)在已知 microRNA 調(diào)控在多細(xì)胞生物中是普遍存在的。
微小 RNA 的調(diào)控機(jī)制已經(jīng)存在了數(shù)十億年,使越來越復(fù)雜的生物體能夠進(jìn)化。研究表明,沒有微小 RNA,細(xì)胞和組織就無法正常發(fā)育。
微小 RNA 的異常調(diào)節(jié)可能導(dǎo)致癌癥,編碼微小 RNA 的基因突變已被發(fā)現(xiàn)會(huì)導(dǎo)致人類先天性聽力損失、眼睛和骨骼疾病。
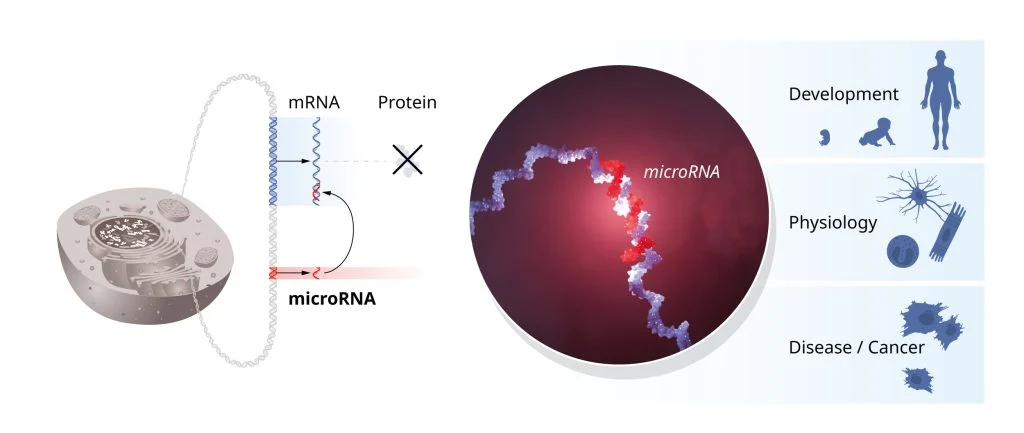
注:microRNA 的開創(chuàng)性發(fā)現(xiàn)是出乎意料的,它揭示了基因調(diào)控的新維度。
為干細(xì)胞再生和治療鋪平道路
在當(dāng)今生命科學(xué)領(lǐng)域,干細(xì)胞治療作為一種充滿希望的前沿療法,正吸引著眾多科學(xué)家的目光。而其中,微小 RNA(miRNA)的發(fā)現(xiàn)為干細(xì)胞治療帶來了新的曙光,展現(xiàn)出巨大的潛力。
調(diào)控干細(xì)胞特性
miRNA 在干細(xì)胞的增殖、分化等關(guān)鍵過程中發(fā)揮著至關(guān)重要的作用,深刻影響著干細(xì)胞的特性。干細(xì)胞作為具有自我更新和多向分化潛能的細(xì)胞,其行為受到精細(xì)的調(diào)控,而 miRNA 正是這一調(diào)控網(wǎng)絡(luò)中的關(guān)鍵節(jié)點(diǎn)。
miRNA 能夠調(diào)節(jié)包括代謝、生長、發(fā)育、免疫等在內(nèi)的各種生物學(xué)功能,從而對細(xì)胞行為產(chǎn)生廣泛影響。例如,miR-34a 能夠限制多能干細(xì)胞獲得擴(kuò)增的細(xì)胞命運(yùn)潛力,其缺陷可擴(kuò)展干細(xì)胞具有同時(shí)發(fā)育成為胚胎和胚外譜系的發(fā)展?jié)摿?。
這種對干細(xì)胞特性的調(diào)控作用,為我們在干細(xì)胞治療中實(shí)現(xiàn)精準(zhǔn)的細(xì)胞命運(yùn)引導(dǎo)提供了有力的工具。通過調(diào)節(jié)特定 miRNA 的表達(dá)水平,我們可以有針對性地控制干細(xì)胞的增殖和分化方向,使其更好地適應(yīng)不同疾病的治療需求。
增強(qiáng)免疫調(diào)節(jié)
除了調(diào)控干細(xì)胞特性,miRNA 還在調(diào)節(jié)干細(xì)胞的免疫抑制功能方面發(fā)揮著重要作用。間充質(zhì)干細(xì)胞在受到炎癥因子刺激后,會(huì)上調(diào) miR-155 的表達(dá),進(jìn)而調(diào)節(jié)其對 T 細(xì)胞增殖的抑制作用。這一過程展示了 miRNA 在干細(xì)胞與免疫系統(tǒng)相互作用中的關(guān)鍵角色。
此外,干細(xì)胞源性外泌體中的 miRNA 通過細(xì)胞間通訊調(diào)節(jié)靶細(xì)胞功能,在免疫調(diào)節(jié)中發(fā)揮著重要作用。外泌體作為細(xì)胞間通訊的重要載體,攜帶了豐富的 miRNA 等生物活性分子。這些 miRNA 可以被受體細(xì)胞攝取,從而調(diào)節(jié)受體細(xì)胞的功能。在干細(xì)胞治療中,外泌體中的 miRNA 可以通過調(diào)節(jié)免疫細(xì)胞的活性,增強(qiáng)干細(xì)胞的免疫抑制功能,為治療免疫相關(guān)疾病提供新的策略。
促進(jìn)組織修復(fù)與再生
通過調(diào)節(jié)干細(xì)胞功能,miRNA 有助于促進(jìn)受損組織的修復(fù)與再生,為治療多種疾病提供了新途徑。當(dāng)組織受到損傷時(shí),干細(xì)胞可以被動(dòng)員到損傷部位,通過分化為特定的細(xì)胞類型,參與組織的修復(fù)過程。而 miRNA 可以通過調(diào)控干細(xì)胞的增殖、分化和遷移等行為,促進(jìn)干細(xì)胞更好地發(fā)揮其修復(fù)作用。
例如,在心肌梗死等心血管疾病中,通過調(diào)節(jié)特定 miRNA 的表達(dá),可以促進(jìn)心肌干細(xì)胞的增殖和分化,促進(jìn)心肌組織的修復(fù),改善心臟功能。在神經(jīng)損傷等疾病中,miRNA 也可以調(diào)節(jié)神經(jīng)干細(xì)胞的分化方向,促進(jìn)神經(jīng)組織的再生。
細(xì)胞治療的新希望
細(xì)胞治療作為一種前沿的醫(yī)療手段,具有巨大的潛力,可以為許多難治性疾病帶來新的希望。然而,細(xì)胞治療的發(fā)展一直面臨著諸多挑戰(zhàn),其中之一就是如何精確地調(diào)控細(xì)胞的功能和命運(yùn)。
miRNA 的發(fā)現(xiàn)為解決這一難題提供了有力的工具。通過調(diào)控 miRNA 的表達(dá),可以實(shí)現(xiàn)對細(xì)胞的精準(zhǔn)調(diào)控,提高細(xì)胞治療的效果和安全性。
個(gè)性化醫(yī)療的未來
miRNA 的獨(dú)特性質(zhì),使得它成為了個(gè)性化醫(yī)療的理想選擇。每個(gè)人的 miRNA 表達(dá)譜都有所不同,這為醫(yī)生提供了一個(gè)個(gè)性化的治療靶點(diǎn)。通過檢測患者的 miRNA 表達(dá)水平,醫(yī)生可以制定出更加精準(zhǔn)的治療方案,實(shí)現(xiàn)個(gè)性化醫(yī)療的目標(biāo)。
多學(xué)科的融合與創(chuàng)新
miRNA 的研究涉及到生物學(xué)、醫(yī)學(xué)、化學(xué)等多個(gè)學(xué)科領(lǐng)域,需要不同領(lǐng)域的科學(xué)家們共同合作,才能推動(dòng)這一領(lǐng)域的不斷發(fā)展。諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)的授予,將進(jìn)一步促進(jìn)多學(xué)科的融合與創(chuàng)新,為細(xì)胞治療的發(fā)展注入新的活力。
總之,miRNA 在干細(xì)胞治療中展現(xiàn)出了巨大的潛力。通過調(diào)控干細(xì)胞特性、增強(qiáng)免疫調(diào)節(jié)和促進(jìn)組織修復(fù)與再生,miRNA 為干細(xì)胞治療提供了新的思路和方法。隨著對 miRNA 與干細(xì)胞相互作用機(jī)制的深入研究,我們有理由相信,miRNA 將在未來的干細(xì)胞治療中發(fā)揮更加重要的作用,為人類健康帶來更多的希望。
2024 年諾貝爾生理學(xué)或醫(yī)學(xué)獎(jiǎng)的授予,是對兩位 miRNA 發(fā)現(xiàn)者的崇高敬意,也是對整個(gè)生命科學(xué)領(lǐng)域的巨大鼓舞。讓我們共同期待,miRNA 的研究將為細(xì)胞治療帶來更多的突破,為人類的健康事業(yè)開創(chuàng)更加美好的未來。
免責(zé)聲明:我們尊重原創(chuàng),也注重分享。圖文來源網(wǎng)絡(luò),版權(quán)歸原作者所有,如涉及作品內(nèi)容、版權(quán)或其它問題,請聯(lián)系我們刪除!


 閩公網(wǎng)安備 35020602002648 號(hào)
閩公網(wǎng)安備 35020602002648 號(hào) QQ 客服
QQ 客服
