北京時間 10 月 2 日,瑞典卡羅林斯卡醫(yī)學(xué)院諾貝爾獎委員會宣布,匈牙利科學(xué)家卡塔林·卡里科(Katalin Karikó)和美國科學(xué)家德魯·韋斯曼(Drew Weissman)榮膺 2023 年諾貝爾生理學(xué)或醫(yī)學(xué)獎,以表彰他們在核苷堿基修飾方面的發(fā)現(xiàn),這些發(fā)現(xiàn)使針對新冠感染的有效信使核糖核酸(mRNA)疫苗的開發(fā)成為可能。他們將平均分享 1100 萬瑞典克朗的獎金。

諾貝爾官方新聞稿表示,這兩位諾貝爾獎獲得者的發(fā)現(xiàn)對于在 2020 年初開始的新冠肺炎大流行期間開發(fā)有效的 mRNA 疫苗至關(guān)重要。通過他們的突破性發(fā)現(xiàn),從根本上改變了人們對信使核糖核酸如何與免疫系統(tǒng)相互作用的理解,獲獎?wù)邽橐呙玳_發(fā)的空前速度做出了貢獻。
免疫治療
說到癌癥治療,很多人的第一反應(yīng)就是化療,脫發(fā)、嘔吐、骨髓抑制等副作用也令人恐懼。但事實上,隨著治療手段的發(fā)展,除了傳統(tǒng)的手術(shù)、放化療之外,靶向治療和免疫治療也逐漸進入人們的視野,尤其是對于一些特殊疾病。這兩種新興的治療方法甚至被公認(rèn)為一線治療方法,其中免疫療法攻擊癌細(xì)胞是因為它不使用外力。相反,它通過培養(yǎng)和治療患者體內(nèi)的免疫細(xì)胞來攻擊腫瘤細(xì)胞,這與傳統(tǒng)療法有很大不同。它能快速、持久地清除大量腫瘤細(xì)胞,減輕患者體內(nèi)腫瘤細(xì)胞的負(fù)荷,備受關(guān)注。
隨著免疫負(fù)調(diào)節(jié)的抗 CTLA-4 和抗 PD-1 抗體在腫瘤研究中的顯著療效,免疫治療掀起了癌癥治療的一場革命。這種療法可以永久消除殘留在體內(nèi)的少量散在腫瘤細(xì)胞,改善因放化療而受損的機體免疫功能。與三種常規(guī)療法聯(lián)合應(yīng)用顯示出互補優(yōu)勢。通過大量的臨床實踐,免疫治療在各種腫瘤的治療中顯示出了良好的應(yīng)用前景,可以提高治療效果,延長生存時間,改善腫瘤患者的生活條件,提高生活質(zhì)量,有望實現(xiàn)腫瘤長期生存或腫瘤完全治愈的目標(biāo)。
談到免疫治療,很多人認(rèn)為免疫治療是提高免疫力的療法,或者認(rèn)為免疫治療是 PD-1(免疫檢查點抑制劑)。實際上,免疫療法遠不止于此。目前,腫瘤的免疫治療可分為四類:免疫檢查點抑制劑(PD-1/PD-L1)、腫瘤疫苗(Provenge/CIMAvax-EGF)、細(xì)胞免疫療法(CAR-T)和非特異性免疫調(diào)節(jié)劑。
01 免疫檢查點抑制劑
首先,最成熟的免疫治療類別是免疫檢查點抑制劑。一般來說,當(dāng)體內(nèi)產(chǎn)生腫瘤細(xì)胞時,強大的免疫系統(tǒng)應(yīng)該會識別并攻擊它們。但是,由于免疫細(xì)胞可以產(chǎn)生抑制自身的小蛋白質(zhì)分子,這種分子可以保證正常身體不會被免疫系統(tǒng)意外傷害。然而,腫瘤細(xì)胞也利用這種機制逃離人體免疫系統(tǒng)而存活。檢查點抑制劑可以緩解這種抑制,重新激活免疫細(xì)胞,消除癌細(xì)胞。
說到免疫檢查點抑制劑的作用機制,就不得不提到 PD-1/PD-L1 抑制劑。其中,“PD-1”抑制(“O”類藥物、“K”類藥物等)和“PD-L1”抑制劑。這兩種藥物都是注射劑,抗腫瘤機制基本相同。由于 PD-1 受體是腫瘤細(xì)胞逃避免疫攻擊的最關(guān)鍵環(huán)節(jié),因此無法識別活化的 T 淋巴細(xì)胞。其中,PD-1 和 PD-L1 蛋白起著關(guān)鍵作用。PD-1 和 PD-L1 分別位于活化的 T 淋巴細(xì)胞和腫瘤細(xì)胞表面。一旦兩者結(jié)合,T 淋巴細(xì)胞將把腫瘤細(xì)胞當(dāng)作正常生物對待,而不會攻擊它們。“PD-1”抑制劑或“PD-L1”抑制劑進入體內(nèi)后可與 PD-1 或 PD-L1 結(jié)合,中斷了腫瘤細(xì)胞隱藏自身的過程,從而使腫瘤細(xì)胞呈現(xiàn)出原來的形態(tài),無法逃脫免疫系統(tǒng)的攻擊。
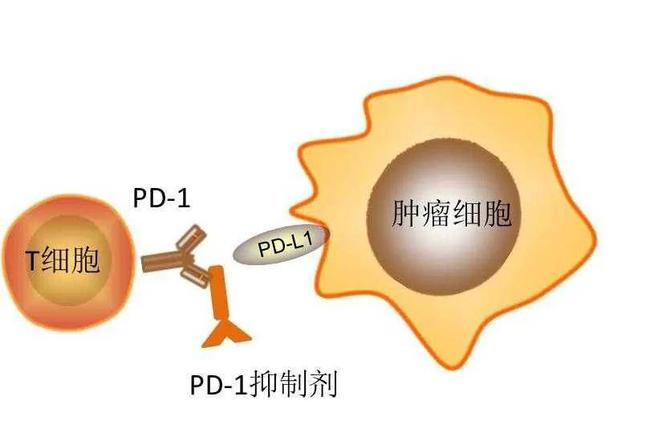
“免疫檢查點抑制劑”等藥物與傳統(tǒng)抗腫瘤藥物有本質(zhì)區(qū)別。它們不是直接針對殺死腫瘤細(xì)胞,而是針對調(diào)節(jié)我們自身的免疫功能。通過改變免疫細(xì)胞與腫瘤細(xì)胞的內(nèi)在聯(lián)系,改變腫瘤細(xì)胞的微環(huán)境,激發(fā)免疫細(xì)胞攻擊腫瘤的巨大潛能,借助自身免疫細(xì)胞殺死腫瘤,從而達到治療腫瘤的最終目的。
02 腫瘤疫苗
腫瘤疫苗也是一種免疫療法。目前,人們首先想到的是新冠病毒疫苗,但實際上,根據(jù)功效的不同,腫瘤疫苗可以分為兩類:一是預(yù)防性疫苗,顧名思義,它是為了預(yù)防健康人腫瘤的發(fā)生。目前市場上有兩類預(yù)防性腫瘤疫苗,包括人乳頭瘤病毒(HPV)疫苗和乙肝病毒(HBV)疫苗。其次,治療性疫苗用于腫瘤治療,也可與手術(shù)、放化療聯(lián)合用于腫瘤的輔助治療。
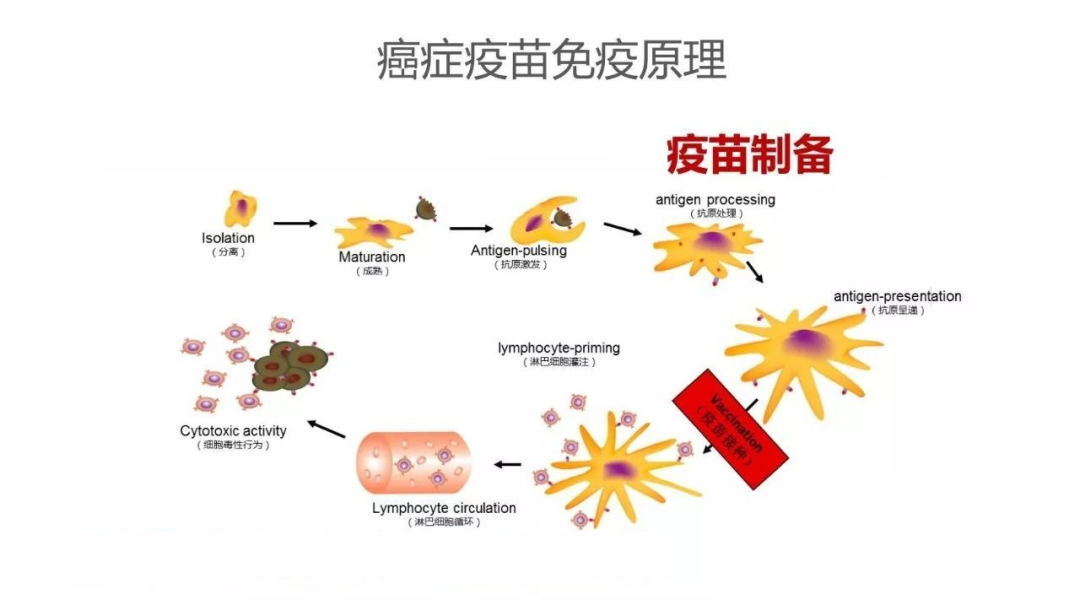
諾貝爾獲獎有關(guān)的 mRNA 疫苗為治療性疫苗。腫瘤疫苗是以各種形式(如核酸、蛋白質(zhì)多肽、細(xì)菌和病毒載體、DC 細(xì)胞等)將腫瘤抗原引入患者體內(nèi)的治療方法。用腫瘤抗原刺激患者體內(nèi)的 T 細(xì)胞,激活患者自身的特異性細(xì)胞免疫。它具有療效高、特異性強、不良反應(yīng)少等優(yōu)點,具有重要的臨床價值。然而,腫瘤疫苗的特點是目前還不成熟,價格昂貴。
03 細(xì)胞免疫療法
CAR-T 細(xì)胞療法,全稱是嵌合抗原受體 T 細(xì)胞免疫療法,是應(yīng)用患者自身的 T 淋巴細(xì)胞,經(jīng)過實驗室重新改造,裝載上具有識別腫瘤抗原的受體及共刺激分子,體外擴增后再次回輸入患者體內(nèi),從而識別并攻擊自身的腫瘤細(xì)胞。
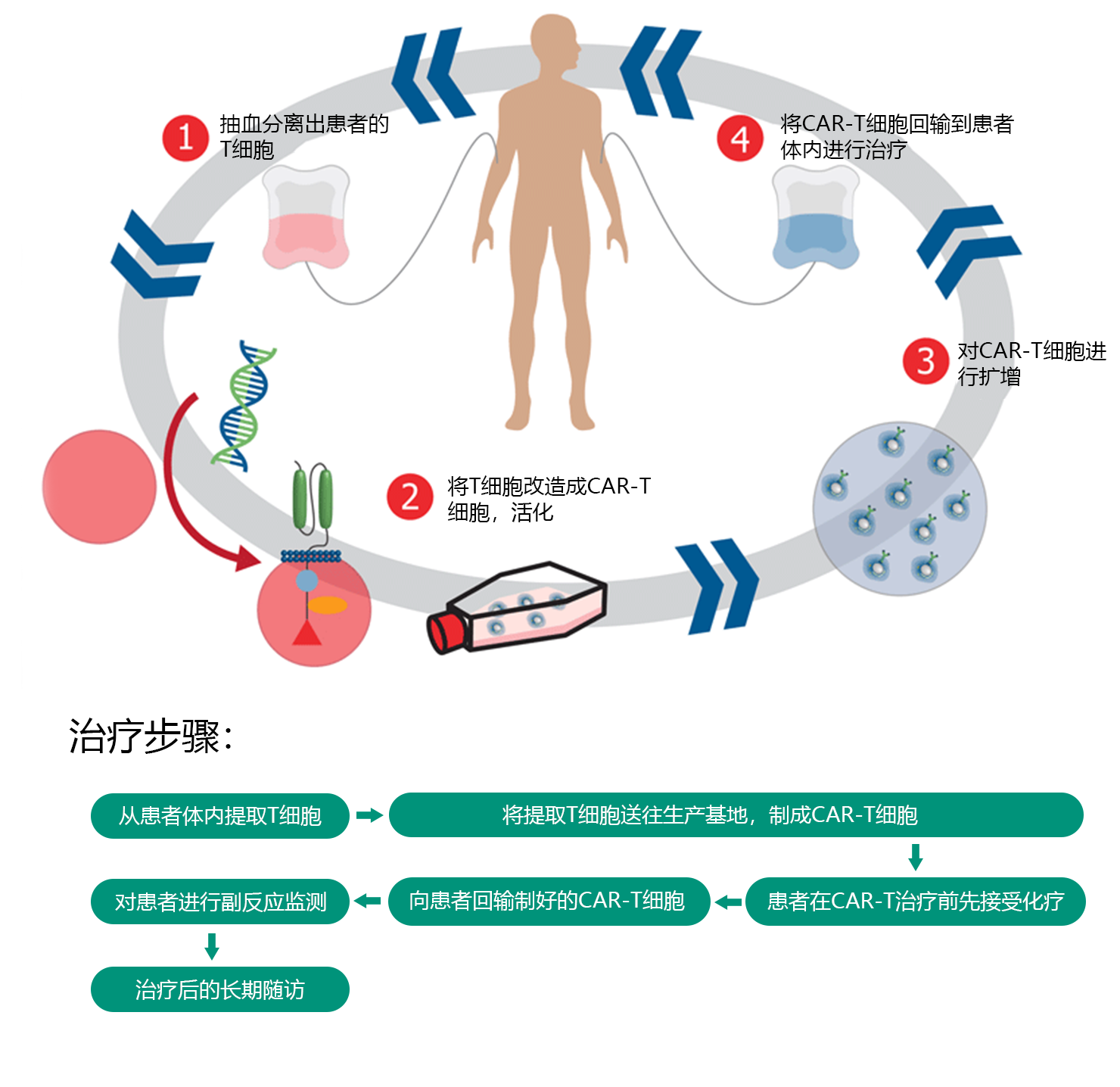
簡單來說,是將患者體內(nèi)的 T 細(xì)胞提取出來,在體外人為地裝上嵌合抗原受體(CAR)——相當(dāng)于給 T 細(xì)胞裝上一個 GPS 導(dǎo)航系統(tǒng),讓 T 細(xì)胞能夠找到腫瘤、消滅腫瘤。在血液腫瘤領(lǐng)域,與手術(shù)、放療、化療等傳統(tǒng)治療方式相比,CAR-T 具有治療更精準(zhǔn)、殺瘤范圍廣、治療次數(shù)少,作用時間長,副作用輕等優(yōu)勢。
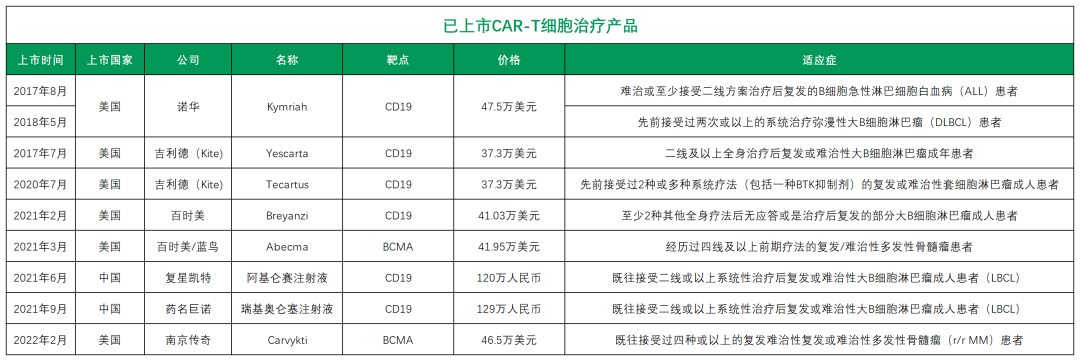
2021 年,阿基侖賽注射液、瑞基奧侖賽注射液先后在中國獲批上市。2022 年西達基奧侖賽被美國 FDA 獲批上市,CAR-T 療法有望進入井噴期。目前,全球共有 9 款 CAR-T 細(xì)胞藥物獲批上市,獲批的適應(yīng)癥也都局限在急性淋巴細(xì)胞白血病、多發(fā)性骨髓瘤、霍奇金淋巴瘤等血液腫瘤領(lǐng)域。
04 非特異性免疫調(diào)節(jié)劑
免疫調(diào)節(jié)劑是一類能增強、促進和調(diào)節(jié)免疫功能的非特異性生物制品,它對治療免疫功能低下、某些繼發(fā)性免疫缺陷癥和某些惡性腫瘤等疾病具有一定的作用,但對免疫功能正常的動物及人卻不起什么作用。其主要機制是通過非特異性方式增強 T、B 淋巴細(xì)胞的反應(yīng)性,或是促進巨噬細(xì)胞的活性,也可以激活補體或誘導(dǎo)干擾素的產(chǎn)生。
非特異性免疫調(diào)節(jié)劑的類型 | 代表性品種 |
| 藥用植物的天然免疫調(diào)節(jié)劑 | 人參、枸杞、松花粉等 |
生物體內(nèi)天然存在的一類免疫調(diào)節(jié)劑 | 胸腺素、轉(zhuǎn)移因子等 |
免疫細(xì)胞經(jīng)刺激后分泌的細(xì)胞因子 | 白細(xì)胞介素-2、干擾素等 |
細(xì)菌來源的免疫調(diào)節(jié)劑 | 卡介苗、小棒桿菌等 |
維生素和微量元素類免疫調(diào)節(jié)劑 | 硒、維生素A等 |
mRNA 疫苗
mRNA 疫苗?技術(shù)?啥玩意?
新冠疫苗知道吧
全球最早上市的新冠疫苗知道是哪款嗎?
你說說看唄。
最早上市的就是 mRNA 疫苗!
隨后是滅活疫苗和腺病毒載體疫苗。
哦這樣!

mRNA 疫苗:一個有前景的 idea
在我們的細(xì)胞中,DNA 中編碼的遺傳信息被轉(zhuǎn)移到 mRNA 中,mRNA 被用作蛋白質(zhì)生產(chǎn)的模板。20 世紀(jì) 80 年代,科學(xué)家們開發(fā)出了在沒有細(xì)胞培養(yǎng)的情況下產(chǎn)生 mRNA 的有效方法,即體外轉(zhuǎn)錄。這決定性的一步加速了分子生物學(xué)在多個領(lǐng)域的應(yīng)用發(fā)展。將 mRNA 技術(shù)用于疫苗和治療的想法也開始興起,但存在障礙。
體外轉(zhuǎn)錄的 mRNA 被認(rèn)為是不穩(wěn)定的,難以遞送,需要開發(fā)復(fù)雜的載體脂質(zhì)系統(tǒng)來包裹 mRNA。此外,體外產(chǎn)生的 mRNA 會引起炎癥反應(yīng)。因此,最初開發(fā)用于臨床目的的 mRNA 技術(shù)的熱情有限。
然而,這些障礙并沒有阻止致力于開發(fā)基于 mRNA 技術(shù)的療法的匈牙利生物化學(xué)家 Katalin Karikó。20 世紀(jì) 90 年代初,當(dāng)她還是賓夕法尼亞大學(xué)的助理教授時,盡管說服研究資助者相信其項目的重要性遇到了困難,但她仍然堅持自己將 mRNA 作為一種治療手段的愿景。
Karikó 在賓夕法尼亞大學(xué)的一位新同事是免疫學(xué)家 Drew Weissman,Weissman 對在免疫監(jiān)視和疫苗誘導(dǎo)的免疫應(yīng)答激活中具有重要功能的樹突狀細(xì)胞感興趣。在新想法的推動下,兩人很快開始了富有成效的合作,重點研究不同類型的 RNA 如何與免疫系統(tǒng)相互作用。
突破性發(fā)現(xiàn)
Karikó 和 Weissman 注意到,樹突狀細(xì)胞將體外轉(zhuǎn)錄的 mRNA 識別為外源物質(zhì),這導(dǎo)致它們的激活和炎癥信號分子的釋放。他們想知道為什么體外轉(zhuǎn)錄的 mRNA 被識別為外來的,而哺乳動物細(xì)胞的 mRNA 卻沒有產(chǎn)生同樣的反應(yīng)。Karikó 和 Weissman 意識到,一些關(guān)鍵特性必定能區(qū)分不同類型的 mRNA。

RNA 包含四個堿基,縮寫為 A、U、G 和 C,對應(yīng)于 DNA 中的 A、T、G 和 C,即遺傳密碼的字母。Karikó 和 Weissman 知道哺乳動物細(xì)胞 RNA 中的堿基經(jīng)常被化學(xué)修飾,而體外轉(zhuǎn)錄的 mRNA 則沒有。他們想知道體外轉(zhuǎn)錄的 RNA 中沒有改變的堿基是否可以解釋這種不必要的炎癥反應(yīng)。為了研究這個問題,他們制造了不同的 mRNA 變體,每種變體的堿基都有獨特的化學(xué)變化,并將其遞送給樹突狀細(xì)胞。結(jié)果是驚人的:當(dāng) mRNA 中包含堿基修飾時,炎癥反應(yīng)幾乎被消除。這是我們對細(xì)胞如何識別和響應(yīng)不同形式 mRNA 的理解的一個范式變化。Karikó 和 Weissman 立即意識到他們的發(fā)現(xiàn)對于使用 mRNA 開發(fā)疾病療法具有深遠的意義。這些開創(chuàng)性成果發(fā)表于 2005 年,比 COVID-19 大流行早了 15 年。

▲兩位諾貝爾獎得主發(fā)現(xiàn),堿基修飾的 mRNA 可以被用來阻斷炎癥反應(yīng)的激活(信號分子的分泌),并在 mRNA 被遞送到細(xì)胞時增加蛋白質(zhì)的產(chǎn)生。
在 2008 年和 2010 年發(fā)表的進一步研究中,Karikó 和 Weissman 表明,與未修飾的 mRNA 相比,遞送包含堿基修飾的 mRNA 顯著增加了蛋白質(zhì)產(chǎn)量。這種效應(yīng)是由于一種調(diào)節(jié)蛋白質(zhì)產(chǎn)生的酶的活性降低。結(jié)合堿基修飾既能減少炎癥反應(yīng),又能增加蛋白質(zhì)的產(chǎn)生這兩方面的重大發(fā)現(xiàn),Karikó 和 Weissman 消除了 mRNA 臨床應(yīng)用道路上的關(guān)鍵障礙。
mRNA 疫苗大放異彩
隨著技術(shù)的突破,人們對 mRNA 療法的興趣開始升溫,2010 年,幾家公司開始致力于開發(fā)這種療法。COVID-19 疫情暴發(fā)后,兩種編碼 SARS-CoV-2 表面蛋白的堿基修飾 mRNA 疫苗以創(chuàng)紀(jì)錄的速度被開發(fā)出來。Karikó 和 Weissman 的發(fā)現(xiàn)為應(yīng)對這個時代最大的健康危機之一做出了重大貢獻。
mRNA 疫苗開發(fā)的靈活性和速度令人印象深刻,這也為利用新平臺開發(fā)其它傳染病疫苗鋪平了道路。在未來,這項技術(shù)還可能用于遞送治療性蛋白質(zhì)和治療某些類型的癌癥。
mRNA 療法賽道是否會升溫?
一年一度的諾貝爾獎除了是科學(xué)界的盛會,也是資本動向和產(chǎn)業(yè)發(fā)展的風(fēng)向標(biāo)之一。那么,目前全球 mRNA 療法(包含疫苗)的在研現(xiàn)狀如何?
據(jù)醫(yī)藥魔方 NextPharma 數(shù)據(jù)庫,目前全球共有超 540 款 mRNA 療法在研,除了獲批上市的近 10 款 COVID-19 mRNA 疫苗,還有 220 個項目處于臨床開發(fā)或申報上市階段。全球來看,在新冠疫苗之后,mRNA 療法在 RSV 疫苗(Moderna 的 mRNA-1345 已經(jīng)申報上市)、流感疫苗(BioNTech/Pfizer 的 PF-07252220、Moderna 的 mRNA-1010 均已進入 III 期臨床)、治療性腫瘤疫苗(Moderna/默沙東的癌癥疫苗 mRNA-4157 已進入 III 臨床)等領(lǐng)域均已取得了重要進展。
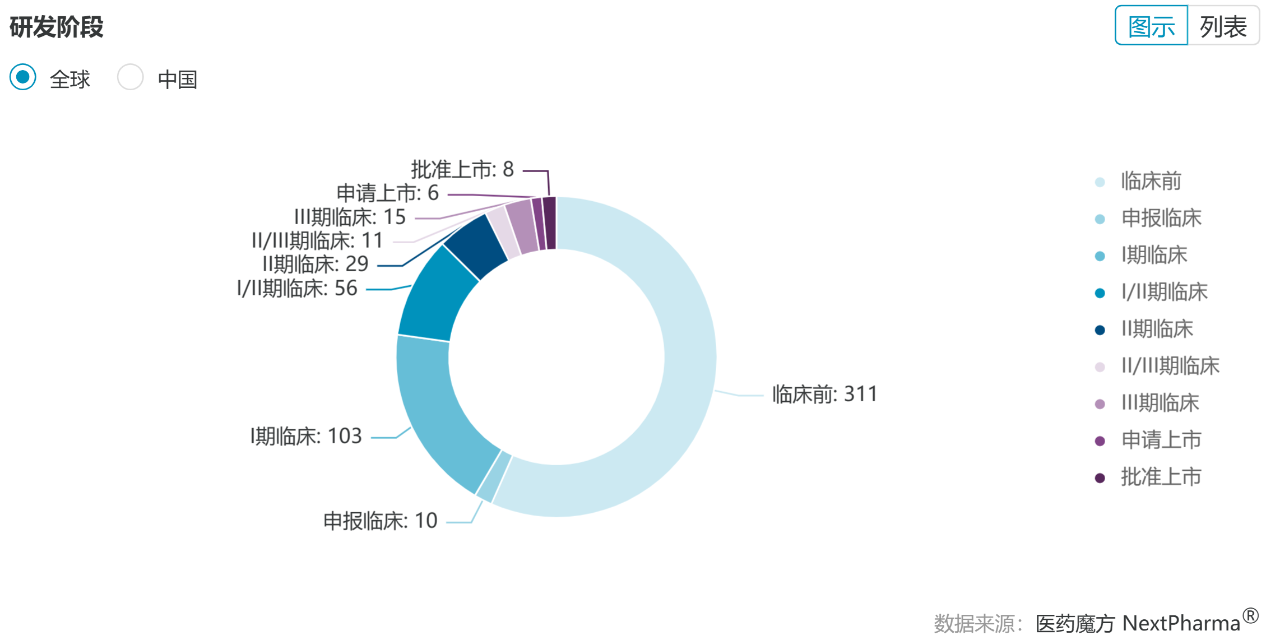
▲全球 mRNA 療法研發(fā)概覽
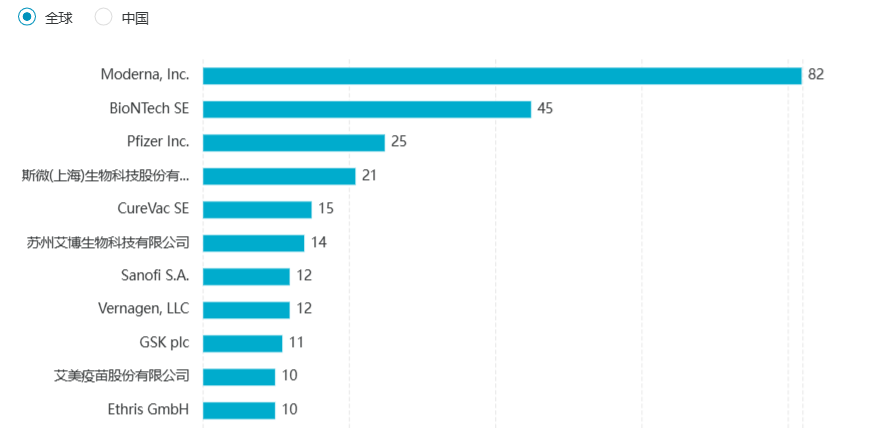
▲ mRNA 療法 TOP10 研發(fā)機構(gòu)
國內(nèi)方面,目前有近 150 個項目同步在研,主要在研適應(yīng)癥為感染性疾病和腫瘤。
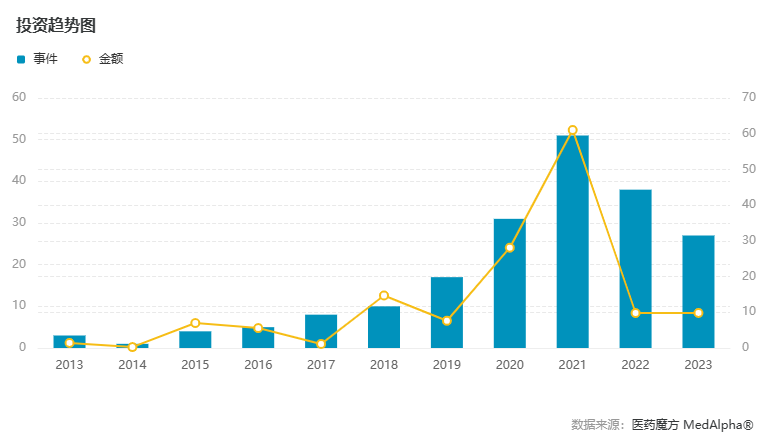
▲ 2013-2023 年 mRNA 療法投資趨勢
資本層面,mRNA 療法賽道在經(jīng)歷了新冠時期的熱火朝天后在這兩年的寒冬下,已逐漸回歸冷靜。這種冷靜從投融資數(shù)量、金額、合作交易等各個維度均有反應(yīng)。在 2023 年諾貝爾生理學(xué)或醫(yī)學(xué)獎的推動下,mRNA 療法賽道能否煥發(fā)新的生機,重拾投資者的興趣及信心,且看未來半年、一年的數(shù)據(jù)給出怎樣的答案。
免責(zé)聲明:我們尊重原創(chuàng),也注重分享。圖文來源網(wǎng)絡(luò),版權(quán)歸原作者所有,如涉及作品內(nèi)容、版權(quán)或其它問題,請聯(lián)系我們刪除!


 閩公網(wǎng)安備 35020602002648 號
閩公網(wǎng)安備 35020602002648 號 QQ 客服
QQ 客服
